РОССИЙСКИЙ ОНКОЛОГИЧЕСКИЙ ЖУРНАЛ. 2019; 24 (1-2) DOI: http://dx.doi.org/10.18821/1028-9984-2019-24-1-2-56-64
КОНФЕРЕНЦИИ И СЪЕЗДЫ
нием ультразвукового исследования и магнитно-резонансной томографии позволяет с большой точностью определить степень распространения опухолевого процесса в мягкие ткани и органы шеи, что позволяет точно определить прогноз и тактику лечения в отношении каждого пациента. Так, для оценки инвазии опухоли в соседние структуры большей диагностической точностью обладает МРТ, в то время как для диагностики метастатического поражения лимфатических узлов шеи большей точностью обладает УЗИ. А также на сегодняшний день современные возможности анестезиологического сопровождения и хирургического оснащения позволяют выполнять большие реконструк-тивно-пластические операции с минимальными осложнениями.
Чойнзонов Е.Л., Чижевская С.Ю., Грибова О.В. НЕЙТРОННО-ФОТОННАЯ ТЕРАПИЯ В КОМБИНИРОВАННОМ ЛЕЧЕНИИ БОЛЬНЫХ РАКОМ ЩИТОВИДНОЙ ЖЕЛЕЗЫ
НИИ онкологии Томского НИМЦ, г. Томск
Актуальность. Эпидемиологические исследования последних десятилетий свидетельствуют об увеличении заболеваемости раком щитовидной железы (РЩЖ) в мире. Заболеваемость раком щитовидной железы в России с 2005 по 2015 г. выросла на 16,53% — с 4,42 до 5,47 на 100 тыс. населения.
Быстрые нейтроны обладают высокими значениями линейной передачи энергии и относительной биологической эффективности. Это обеспечивает уменьшение зависимости повреждения опухоли от фазы клеточного цикла и степени насыщения кислородом, снижение репарации сублетальных повреждений.
Цель исследования — повышение эффективности лечения больных злокачественными опухолями щитовидной железы с применением нейтронно-фотонной терапии.
Материалы и методы. Под нашим наблюдением находились 45 пациентов с морфологически верифицированным РЩЖ Ш-ГУ стадии опухолевого процесса. Показания к проведению нейтронно-фотонной терапии при РЩЖ в послеоперационном периоде:
• распространение опухоли за пределы капсулы, инвазия в прилежащие ткани;
• наличие остаточной опухоли после оперативного вмешательства;
• неблагоприятные морфологические варианты — ана-пластический, плоскоклеточный, медуллярный РЩЖ;
• низкодифференцированные формы РЩЖ. Лучевая терапия начинается через 10-14 дней после
операции. Методика проведения нейтронной терапии:
• 1 поле 8^6 см — на «ложе» щитовидной железы;
• 1 поле 6^8 — 10×10 см — на «ложе» удалённых метастатических л/узлов шеи с каждой стороны. Режим: РОД 1,4-2,0 Гр, СОД 3,2 — 7,2 Гр (14-34
изоГр). Вклад быстрых нейтронов в курсовую СОД 30-50%. Вторым этапом проводится фотонная терапия в стандартном режиме РОД 2,0 Гр до курсовой СОД 50-55 изоГр при послеоперационном курсе лучевой терапии.
Результаты. При анализе отдалённых результатов лечения больных РЩЖ, имеющих неблагоприятные факторы прогноза течения заболевания, получены обнадёживающие результаты. Так, общая 5-летняя выживаемость больных после комбинированного лечения составила 70,2 ± 8,9%, 5-летняя безрецидивная выживаемость — 52 ± 10,6%. Во время проведения нейтронно-фотонной терапии наблюдались лучевые реакции
как и при стандартной лучевой терапии. В послеоперационном периоде преобладали сухие эпидермиты -I степень по RTOG. Также у 35% больных при п/о курсе нейтронно-фотонной терапии имелись явления эзофа-гита и ларингита I степени. Следует отметить, что ни в одном случае не было зафиксировано язв и некрозов кожи и слизистых, а возникающие осложнения купировались с помощью указанных методов и не требовали длительных перерывов в лечении. Поздние лучевые повреждения кожи и подкожной клетчатки I—II степени после нейтронно-фотонной терапии составили 37%. Лучевые повреждения подкожной клетчатки ограничивались склерозом, фиброзом, истончением подкожно-жирового слоя, телеангиоэктазиями.
Таким образом, нейтронная терапия имеет преимущество при лечении радиорезистентных опухолей по сравнению со стандартными методами, применяемыми в онкологической практике.
В то же время, ввиду особенностей распределения быстрых нейтронов в тканях, применение нейтронной терапии сопряжено с повышенным уровнем осложнений. Одним из путей решения этой проблемы является использование смешанной нейтронно-фотонной терапии. Это позволяет сохранить преимущества плотно-ионизирующего излучения и снизить количество осложнений. Ни в одном случае не зафиксировано развития язв и некрозов кожи и слизистых, а возникающие осложнения купировались с помощью физиотерапевтических и симптоматических методов и не требовали длительных перерывов в лечении.
Выводы. Таким образом, опыт применения нейтронной терапии у больных РЩЖ показал удовлетворительную переносимость. Умеренно выраженные лучевые реакции легко купируются и не требуют длительных перерывов в лечении. Получены обнадёживающие результаты лечения больных с неблагоприятными факторами прогноза РЩЖ (общая 5-летняя выживаемость больных после комбинированного лечения составила 70,2±8,9%).
КожановЛ.Г., Сдвижков А.М., Романова Е.С. ОШИБКИ В ДИАГНОСТИКЕ И ЛЕЧЕНИИ РАКА ЩИТОВИДНОЙ ЖЕЛЕЗЫ
ГБУЗ «ОКД №1» ДЗ г. Москвы
Проблема диагностики и лечения РЩЖ является сложной и противоречивой, в связи с особенностями клинического течения заболевания, трудностями точной цитологической и гистологической интерпретации опухоли, отсутствием системного подхода к диагностике, выбору метода лечения, объёму оперативного вмешательства и диспансерного наблюдения.
На основании проведённых исследований нами установлены причины диагностических и лечебных ошибок:
• Отсутствие онкологической настороженности и незнание особенностей клинического течения РЩЖ.
• Несоблюдение принципов обязательного полного обследования больного (гормональный профиль, сканирование ЩЖ J137, пертехнататом Тс99, УЗИ с использованием современных методик, а также УЗИ с обязательным проведением тонкоигольной аспирационной биопсии — ТАБ).
• Планирование лечения осуществляется одним врачом, а не консилиумом специалистов (эндокринолог, хирург-онколог, радиолог).
• Лечение, в том числе хирургическое, осуществля-
RUSSIAN JOURNAL OF ONCOLOGY. 2019; 24 (1-2) DOI: http://dx.doi.org/10.18821/1028-9984-2019-24-1-2-56-64
ется врачами, не имеющими достаточного опыта в проведении подобного рода операций. Кроме того определены тактические ошибки, к которым относятся:
• длительное наблюдение без лечения (63%),
• гормонотерапия без верификации диагноза (37%),
• неадекватное оперативное вмешательство (38,7%). Операции по поводу РЩЖ должны выполняться по
следующим онкологическим принципам:
• доля, в которой локализуется раковая опухоль, должна быть удалена полностью;
• удаление доли или ЩЖ выполняется экстрафасци-ально;
• при выявлении метастазов на шее и передне-верхнем средостении выполняется операция на первичном очаге и лимфопутях.
Оперативные вмешательства, произведённые с нарушением этих принципов, подразделяются:
• нерадикальные — выявляется опухоль в оставшейся доле ЩЖ;
• неадекватные — отсутствуют признаки опухоли в оставшейся части доли ЩЖ.
По нашим данным, первая нерадикальная операция выполнялась на основании пальпации и клинического обследования у 79% больных, УЗИ проведено у 21%, пункция опухоли у 20%. Эти больные РЩЖ ранее были оперированы в различных учреждениях с нарушением принципов радикализма: энуклеация опухоли, интрафасциальная резекция, удаление одного из метастазов в лимфоузлах шеи.
Неадекватность и нерадикальность выполненной операции при РЩЖ диктовали необходимость выполнения повторных хирургических вмешательств, которые сопряжены с увеличением объёма оперативного вмешательства, проведением дополнительных методов лечения и увеличением количества осложнений.
Таким образом, различные подходы к диагностике и лечению РЩЖ онкологов, хирургов, эндокринологов, лучевых специалистов нуждаются во всестороннем обсуждении этой проблемы и выработке общей тактики диагностики и лечения.
Новожилова Е.Н., Сергеев С.А., Ольшанская О.В., Косташ О.В.
ПОКАЗАНИЯ К ПОВТОРНЫМ ОПЕРАЦИЯМ ПРИ РАКЕ ЩИТОВИДНОЙ ЖЕЛЕЗЫ
Московская городская онкологическая больница № 62 (гл. врач Д. Ю. Каннер)
Введение. В последние годы продолжается рост заболеваемости РЩЖ. За 10 лет заболеваемость возросла более чем в 2 раза. Сложность радикального лечения РЩЖ обусловлена тем, что пациентов оперируют в различных лечебных учреждениях нередко с первоначальным диагнозом «зоб» или «аденома». Нередко о диагнозе рака хирург узнает только после получения планового гистологического исследования, когда больной уже выписан из стационара. Здесь и возникает вопрос о необходимости повторной операции.
Материалы и методы. Операции, выполненные с нарушением онкологических принципов, делятся на нерадикальные (когда в оставшейся части железы определяется остаточная опухоль) и неадекватные (когда при обследовании данных остаточной опухоли нет). При нерадикальных операциях сомнений в необходимости повторного вмешательства не возника-
CONFERENCES AND CONGRESSES
ет. Особые трудности для онколога возникают после неадекватных операций, когда клинические признаки остаточной опухоли отсутствуют.
Нами проанализированы сведения 335 больных РЩЖ, у 62,3% из них при повторной операции остаточная опухоль не была обнаружена. Поэтому мы рассмотрели детально группу из 140 пациентов, которым повторные вмешательства после неадекватной операции не выполнялись, и они были оставлены под динамическим наблюдением.
Результаты. При анализе информации о 140 больных установлено, что у 89,3% (125) были I—II ст. заболевания и высокодифференцированные формы опухоли. Наиболее прогностически неблагоприятным фактором являлась инвазия капсулы железы, при которой рецидив возникал в 100% случаев. После резекции доли рецидив выявлен у 37,8%. Надёжным инструментом для определения показаний к повторной операции является УЗИ с пункцией. Разрешающая способность этого метода достигает 86,5%. Время повторной операции варьировало от 6 мес. до 8 лет. Остаточная раковая опухоль при повторных операциях была выявлена у 61,4% (86), у 11,2% из них выявлены паратрахеальные метастазы. При этом у 38,6% — данных о наличии опухоли не обнаружено (хотя при УЗИ выявлены включения различной эхогенности).
В настоящее время всё большее распространение приобретают молекулярно-генетические исследования, которые позволяют изначально выявить формы новообразований с высоким злокачественным потенциалом (например, BRAF — мутированные формы).
Выводы. Необходимо оптимизировать показания к повторным операциям при РЩЖ без ущерба радикализму лечения. Несомненно существует часть больных, которых возможно оставить под строгим динамическим наблюдением после неадекватных вмешательств. Наиболее значимыми критериями, позволяющими прогнозировать развитие рецидива являются: инвазия капсулы железы, понижение диф-ференцировки опухоли, локализация узла в нижнем сегменте доли, наличие паратрахеальных метастазов. УЗИ с прицельной диагностической пункцией, выполненное в онкологическом учреждении, имеет высокую разрешающую способность и является надёжным инструментом при планировании объёма операции. Молекулярно-генетические исследования, несомненно, получат всё более широкое распространение как при первичной диагностике опухолей, так и при прогнозировании течения заболевания и в определении показаний к повторным операциям.
Письменный В.И., Письменный И.В. РАСПРОСТРАНЁННЫЙ РАК ЩИТОВИДНОЙ ЖЕЛЕЗЫ. ТАКТИКА, МЕТОДЫ ЛЕЧЕНИЯ, КАЧЕСТВО ЖИЗНИ
Самарский государственный медицинский университет; Дорожная клиническая больница, г. Самара
Введение. Доля РЩЖ составляет 0,5% среди всех новообразований у мужчин и 1% — у женщин. В то же время РЩЖ — это самая распространённая опухоль органов эндокринной системы человека. Экстратиреоид-ная инвазия при высокодифференцированных формах РЩЖ встречается в 4-24% наблюдений. Сложность задач, которые необходимо решать при хирургическом лечении распространённого РЩЖ с выходом опухоли
1770 просмотров
23 июня 2020
Доброго времени суток, уважаемые врачи!
Мне 28 лет. 4 года назад начала наблюдать у эндокринолога по вопросу гормонов. Поставили диагноз признаки аутоиммунного тиреодита. узлы левой доли щитовидной железы. По последнему узи: размеры правой доли 50*16*19 мм левой доли 51*15*17. В нижней трети левой доли узел смешанной эхогенности (гипоэхогенный с более эхогенной центральной частью) размерами 14*9*14 с капсулой, в режиме ЦДК картируется перинодулярный кровоток, объемом 0,9 куб.см. 5 баллов по TI-RADS, TR-4. Так же в левой доле лоцируются зоны пониженной эхогенности — в средней трети 5*6*4 мм и верхней трети 4*5*5, без капсулы, с нечеткими границами, в режиме ЦДК кровоток не картируется. Лимфоузлы не изменены.
Соответственно с таким узлом я пошла на биопсию. Результат: цитологическая картина папиллярной карциномы щитовидной железы. Bethesda VI. Врач сказал рак, надо удалять. Но из-за карантина по короновируса я не смогла сразу попасть на операционный стол. Пока ждала снятия ограничений по карантину решила пересдать биопсию в другой клиники. Тот же узел, но теперь результат :на фоне обильного жидкого коллоида определяется небольшое количество тиреоцидов с выраженными дистрофическими изменениями, расположенными разрозненно и многочисленными пеннистыми клетками. Бетесда II узлового, преимущественно коллоидного зоба с признаками кистозной дегенерации. Врач сказал рака нет, не переживай, можно планировать беременность и жить спокойно. Предложил ЛИТТ.
Забрав свои стекла из обоих лаборатирой. Я сдала их в третью стороннию лабораторию. По результатам их исследования подтверждается, что в первом случае Bethesda V подозрение на злокачественное поражение с признаками кистозной дегенерации; по вторым стеклам: картина коллоидного зоба с кистозной дегенерации Bethesda II доброкачетсвенный процесс.
И вопрос как мне быть кому верить?! идти на операцию или сдавать еще третью биопсию?! Может ли быть что в первом случаи в узле попали именно в раковые клетки, поэтому такой результат. А во втором-промахнулись и не попали.
Принимаю лтироксин 100 через день. ТТГ 2,36 мкМЕ/мл, Т4 свободный 15,8 пмоль/л
Надеюсь получить от Вас совет и ответ на вопрос: может ли быть различный результат только потому, что забор был из разных частей одного и того же узла.
На сервисе СпросиВрача доступна консультация эндокринолога онлайн по любой волнующей Вас проблеме. Врачи-эксперты оказывают консультации круглосуточно и бесплатно. Задайте свой вопрос и получите ответ сразу же!

Эндокринолог, Сомнолог
Здравствуйте конечно возможно, что второй раз клетки не попали в иглу. Если хотя бы есть подозрения на карциному, нужно удалять. 100% покажет только гистология удаленного узла. Есть генетическое исследование, которое 99% покажет по смыву со стекол, но доступно оно в Новосибирском институте генетики. Модно пересмотреть стекла у цитологов именно онкодиспансера, у них опыта больше.
Анастасия, 23 июня 2020
Клиент
Наталия, спасибо за Ваш ответ. Как раз в онкоцентр я и сдавала оба варианта стёкол
Анастасия, 25 июня 2020
Клиент
Наталия, будьте добрый скажите как называется анализ про который Вы писали. Я попробую узнать как его сдавать и съездить в Новосибирск
Анастасия, 25 июня 2020
Клиент
Наталия, и Контакты института если Вам известны.
И подскажите этот анализ покажет есть ли у меня рак или нет или он покажет есть ли у меня предрасположенность к раку?!

Эндокринолог, Сомнолог
Подскажет конкретно, рак ли это. Институт Молекулярной генетики. Не знаю, можно ли здесь размещать такие контакты. Отдел структуры и функции хромосом
Лаборатория молекулярной генетики контакты есть у них на сайте.
Анастасия, 26 июня 2020
Клиент
Наталия, а название самого анализа?! И вообще что это кровь, старые стёкла можно сдать или заново биопсию, или мазок какой то?! Просто даже не знаю как объяснить в институте что мне от них нужно

Эндокринолог, Сомнолог
Все стекла, какие есть на молекулярно-генетический анализ — диагностика новообразований щитовидной железы человека.
Анастасия, 26 июня 2020
Клиент
Наталия, спасибо Вам огромное! Буду наводить справки!

Эндокринолог, Сомнолог
Учёные работают с онкоцентрами Санкт-Петербурга, Москвы, Томска, Ульяновска, Краснодара, Новосибирска. тест система называется «ТИРОИД-1» и позволяет идентифицировать онкологические новообразования со специфичностью 96,8% и чувствительностью 82,7%. Вторая панель — «ТИРОИД-2». Производит «Вектор -Бест»

Эндокринолог, Сомнолог
Прием тироксина через день не приемлемо. Нужен ежедневный прием.
Анастасия, 23 июня 2020
Клиент
Наталия, это самая подходящая дозировка оказалась для меня. Каждый день по 100-много по 75-мало. Вот и эндокринолог предложила пить по 100 через день. И уже в течении года гормоны в норме при такой дозировки

Эндокринолог, Сомнолог
Если 100 мкг через день, получается по 50 мкг ежедневно. Если Вы себя на таком режиме хорошо чувствуете, то можно конечно. Просто максимум действия препарата наступает через 6-8 часов, затем снижается постепенно. После удаления железы лучше такой режим не использовать.
Оцените, насколько были полезны ответы врачей
Проголосовало 0 человек,
средняя оценка 0
Что делать, если я не нашел ответ на свой вопрос?
Если у Вас похожий или аналогичный вопрос, но Вы не нашли на него ответ — получите свою медицинскую консультацию онлайн.
Если Вы хотите получить более подробную консультацию врача и решить проблему быстро и индивидуально — задайте платный вопрос в приватном личном сообщении. Будьте здоровы!
- Диагноз Фолликулярная аденома щитовидной железы
- Заключение по результатам ТАБ щитовидной железы
- Где выполнить биопсию щитовидной железы
- Аденома щитовидной железы лечение
- Диагностика аденомы щитовидной железы
ВНИМАНИЕ! Если Вы читаете эту статью потому, что получили заключение тонкоигольной биопсии узла щитовидной железы, сформулированное как “Фолликулярная аденома щитовидной железы», «Атипическая фолликулярная аденома щитовидной железы» или просто «Фолликулярная аденома» или «Аденома щитовидной железы» — Вы должны знать, что диагноз по результатам тонкоигольной биопсии ВАМ УСТАНОВЛЕН НЕПРАВИЛЬНО. И вероятность того, что наше утверждение справедливо – 100%.
В современной всемирной классификации диагнозов по итогам биопсии – The Bethesda system for reporting thyroid cytopathology, последний из вариантов которой был принят на всемирном конгрессе патологов в городе Bethesda (США) в 2010 году диагноза «Фолликулярная аденома щитовидной железы» НЕТ ВООБЩЕ. И нет его там, стоит отметить, уже достаточно давно. И только в России – стране, авторы цитологических руководств в которой упорно продолжают игнорировать мировой опыт, такой диагноз сохраняется. В России активно используется классификация цитологических (биопсийных) диагнозов по Шапиро-Камневой – классификация нелогичная, абсолютно не связанная с окружающей действительность, содержащая массу неизвестных остальной науке заключений.
Поэтому если Вам был установлен диагноз «Фолликулярная аденома щитовидной железы» после проведения тонкоигольной биопсии (а затем, как это обычно бывает, рекомендована операция), то единственный способ для Вас получить качественную диагностику и, если потребуется, лечение в правильные сроки и в правильном объеме – это забрать свои цитологические препараты (в быту их называют часто «стеклами») из того центра, где проводилась биопсия и приехать для консультации в специализированный центр эндокринологии и эндокринной хирургии – Северо-Западный центр эндокринологии в Санкт-Петербурге. Если Вам не отдадут цитологические препараты на руки (что является грубым нарушением прав пациента, но достаточно часто встречается в нашей стране) – приезжайте без «стекол», Вам проведут повторную биопсию прямо в Санкт-Петербурге, а результат ее будет готов уже на следующий день. Особо следует рекомендовать повторную консультацию результатов биопсии тем пациентам, кто получил в качестве заключения диагноз «Атипическая аденома щитовидной железы» — заключение, которое сразу наводит на мысли о некомпетентности цитолога (в нашей практике именно в этой группе заключений при повторной биопсии выявляется наибольшее число диагностических ошибок).
Почему мы так радикальны в своих высказываниях?
Вы можете задать вопрос – почему мы так категорично высказываемся о том, что другие специалисты поставили диагноз обязательно неверно, а также кто мы такие, чтобы высказываться так радикально? И почему мы рекомендуем не повторять биопсию у Вас по месту жительства, а сразу приезжать для повторного исследования в Санкт-Петербург? Давайте попробуем ответить на все три вопроса последовательно.
Почему мы так категоричны, так радикальны?
Ответим на первую часть Вашего вопроса – диагноз фолликулярной аденомы щитовидной железы по результатам тонкоигольной биопсии поставлен быть не может просто потому, что это НЕВОЗМОЖНО. Никто в мире не может надежно установить диагноз фолликулярной аденомы – этот вопрос сейчас является основным научным направлением в диагностике узлов щитовидной железы.
Давайте поясним наше положение с использованием некоторых простых теоретических положений.
Когда мы, эндокринологи и эндокринные хирурги, выявляем у пациента узел в щитовидной железе, мы в первую очередь должны определиться с основным вопросом: «Является этот узел доброкачественным или злокачественным?» Если сказать еще проще и конкретнее: «Рак это или нет?»
Главным методом, позволяющим ответить на этот простой и в то же время крайне важный для пациента вопрос, является тонкоигольная биопсия узлов щитовидной железы. Именно она призвана разделять узлы на опасные для человека и не опасные. Многие пациенты удивятся, но основной целью биопсии является не назначение пациентам операций по удалению узлов, а избавление пациентов от операций. Биопсия позволяет сказать пациенту без всякой операции, что у него – доброкачественный узел (а доброкачественных узлов – 95%), и затем на основании заключения биопсии дать совет не удалять узел и не проводить никаких операций. В те времена, когда биопсии не существовало, врачи рекомендовали удалять все выявленные узлы – иначе они не могли гарантировать пациенту, что у него не будет «пропущен» рак. И сейчас во многих регионах нашей страны (в первую очередь там, где биопсию не делают, либо делают некачественно) врачи рекомендуют удалять практически все узлы. Но врачи при этом часто не могут понять, что к 50 годам у 50% женщин есть узлы в щитовидной железе, и если мы будем двигаться путем их удаления, то к определенному возрасту мы удалим щитовидную железу как минимум половине женщин нашей страны…
Биопсия щитовидной железы позволяет разделить узлы на те, которые необходимо удалять (к счастью, их немного – около 7-8%), и те, которые удалять не следует – их значительно больше, около 92-93%.
Как биопсия это делает?
Первое, что может биопсия – это разделить узлы на опухолевые и неопухолевые. Многие не знают, но все узлы в щитовидной железе делятся, в первую очередь, на опухоли и не-опухоли.
Не-опухоли, которых подавляющее большинство,- это так называемые коллоидные узлы, абсолютно доброкачественные округлые образования, похожие на опухоль, но с точки зрения микроскопического строения опухолью не являющиеся. Единственной проблемой этих узлов является тот факт, что они очень и очень похожи при проведении УЗИ или ощупывании щитовидной железы на опухоль – поэтому их и удаляют так часто. Качественная биопсия позволяет высказаться уверенно, что узел является коллоидным – а значит, не является раком и НИКОГДА в него не «переродится». Доброкачественные коллоидные узлы в рак не превращаются – этот факт наукой доказан уже достаточно давно. И коллоидные узлы составляют около 92-95% от всех узлов щитовидной железы – к большому счастью всего человечества.
Опухолевые узлы щитовидной железы отличаются от коллоидных неопухолевых узлов тем, что в опухолях всегда есть одна «материнская» клетка, в которой произошла вызывающая безудержное деление мутация ДНК. Размножение материнской клетки приводит к образованию узла в щитовидной железе, все клетки которого являются в том или ином поколении потомками материнской клетки (в коллоидном узле такого феномена нет – там делятся все клетки сразу, потому он и является неопухолевым).
Опухолевые узлы в щитовидной железе бывают доброкачественными и злокачественными. Доброкачественный опухолевый узел иначе называют аденомой щитовидной железы, а злокачественный – раком щитовидной железы.
Вторая задача, которую призвана решать тонкоигольная биопсия – это разделение опухолевых узлов на злокачественные и доброкачественные. И с этой задачей биопсия пока может справиться не на 100%.
Ряд злокачественных опухолей биопсия позволяет выявить сразу – например, папиллярный рак, медуллярный рак, плоскоклеточный рак, анапластический рак, лимфому щитовидной железы, метастазы других опухолей в щитовидную железу.
Однако есть два вида опухолей, которые друг от друга по результатам тонкоигольной биопсии не отличимы. Речь идет о фолликулярной аденоме щитовидной железы (доброкачественной опухоли, происходящей из клеток фолликулов, вырабатывающих гормоны) и фолликулярной карциноме щитовидной железы
(или фолликулярном раке – злокачественной опухоли щитовидной железы, растущей все из тех же вырабатывающих гормоны клеток фолликулов).
Почему биопсия не может отличить аденому от карциномы? Дело в том, что клетки, образующие две эти опухоли, одинаковы
– это обычные клетки фолликулов щитовидной железы. При анализе мазка, полученного после тонкоигольной биопсии щитовидной железы, видны скопления фолликулярных клеток, которые активно делятся – и это все, что можно сказать по результатам биопсии. Видно, что узел имеет фолликулярное строение, что он состоит из клеток фолликулов, и эти клетки делятся – значит, речь идет об опухоли. Больше ничего не сказать.
Основным отличием фолликулярного рака от фолликулярной аденомы щитовидной железы является наличие инвазии капсулы в раковых узлах. Дело в том, что обе опухоли – и карцинома (рак), и аденома (доброкачественная опухоль) – покрыты капсулой, которая окружает узел, подобно тонкой оболочке. Клетки аденомы не способны разорвать оболочку и проникнуть в окружающие ткани, а клетки рака (карциномы) делают это достаточно легко. Именно поэтому наличие очагов разрывов капсулы узла с прорастанием (инвазией) клеток опухоли в окружающую ткань является основным признаком фолликулярного рака щитовидной железы. Это – незыблемый, никем не оспариваемый факт. Есть инвазия – это рак, нет инвазии – это фолликулярная аденома.
А теперь давайте подумаем, как можно выявить инвазию капсулы узла опухолью при проведении тонкоигольной биопсии? Ведь биопсия проводится очень тонкой иглой путем укола в ткань узла с последующим всасыванием содержимого узла в шприц, а затем выдуванием этого содержимого на стекло, и потом – размазыванием этого содержимого по стеклу с приготовлением тонкого мазка. Чем тоньше мазок – тем лучше видно отдельные клетки, тем качественнее взята биопсия и тем выше вероятность информативного ответа. Но капсулу узла при биопсии не высосать – это очевидно. И выяснить, как располагались клетки в узле до биопсии, тоже невозможно – ведь они перемешиваются и в игле, и в шприце, и на стекле при размазывании клеточного материала. Поэтому сказать, была ли инвазия опухолью капсулы узла по итогам тонкоигольной биопсии невозможно – для этого необходимо изучить всю капсулу, весь узел. Это так же невозможно, как пытаться выяснить, были ли, допустим, темные точки на шкурке апельсина, путем выпивания полученного из него апельсинового сока через трубочку – чтобы сказать что-то о шкурке апельсина, нужно изучать именно шкурку, а не сок.
Единственный способ сказать, есть ли инвазия опухолью капсулы узла (а значит, решить – является исследуемый узел фолликулярной аденомой щитовидной железы или фолликулярным раком) – это удалить узел целиком и тщательно исследовать всю его капсулу под микроскопом в поисках очагов инвазии, «дырок» в капсуле. Это – логично и это очевидно.
Из приведенных выше рассуждений следует, что по данным тонкоигольной биопсии установить диагнозы «Фолликулярная аденома щитовидной железы» и «Фолликулярный рак щитовидной железы» НЕВОЗМОЖНО. Невозможно не потому, что не хватает знаний врача или оборудования, а невозможно чисто технически. Поэтому такие диагнозы по результатам биопсии формулироваться не могут. И поэтому в современной всемирной классификации Bethesda system 2010-го года выпуска указано, что заключение необходимо формулировать так: «Фолликулярная опухоль щитовидной железы». Т.е. цитолог понимает, что это – опухоль из фолликулярных клеток, он также понимает, что отличить в данном случае рак от аденомы он не может в силу ограничений метода, поэтому он просто пишет общее заключение «Фолликулярная опухоль». Если узел будет удален (а так сейчас и принято поступать со всеми фолликулярными опухолями) и врач получит возможность оценить весь узел с его капсулой, диагноз будет уже установлен окончательно – или рак, или не рак (аденома).
Из этого длинного рассуждения следует два важных вывода.
Первый – диагноз «Фолликулярная аденома щитовидной железы» может быть установлен только после полного удаления узла.
Второе – если цитолог этого не понимает и пишет заключение «Фолликулярная аденома щитовидной железы» по итогам тонкоигольной биопсии, значит, он не понимает самой логики данного метода диагностики, не ориентируется в современных классификациях и правилах установки диагноза, и следовательно – его заключениям доверять нельзя.
Вот именно поэтому мы и сообщили Вам в начале статьи, что диагноз фолликулярной аденомы щитовидной железы по итогам тонкоигольной биопсии узла – это НЕВЕРНЫЙ диагноз, и никаких исключений из этого правила нет.
Вопрос второй – кто мы такие?
Мы – специалисты Северо-Западного центра эндокринологии, расположенного в Санкт-Петербурге и занимающегося диагностикой и лечением заболеваний эндокринных органов: щитовидной железы, паращитовидных желез, надпочечников.
Мы – российские лидеры в области тонкоигольной биопсии узлов щитовидной железы. Ежегодно в нашем центре проводится анализ 25000 биопсий щитовидной железы. Мы также консультируем цитологические препараты из всех регионов Российской Федерации и из-за рубежа.
Мы – российские и европейские лидеры в области хирургии щитовидной железы. Ежегодно в нашем центре проводится более 5000 операций на щитовидной железе. По этому показателю мы находимся на первом месте в России и входим в тройку крупнейших европейских клиник эндокринной хирургии.
Мы – клиника, которая исповедует разумный подход к лечению пациентов с узлами щитовидной железы. Заметьте, мы проводим в год 25000 биопсий и оперируем только 5000 пациентов. Это соотношение между числом биопсий и числом операций (8% узлов удаляется после биопсии) совершенно точно повторяет данные мировых исследований о распространенности рака – 5% от всех узлов составляет рак щитовидной железы и еще 3-4% «дают» фолликулярные аденомы, которые также удаляются. Соотношение очень четкое, очень наглядное. Из него следует одно важное и очевидное заключение – мы практически не оперируем пациентов с доброкачественными коллоидными узлами щитовидной железы. Пациенты с доброкачественными узлами оперируются только в тех случаях, если узлы достигли большого размера и вызывают дискомфорт или косметический дефект (пациент в таком случае сам изъявляет желание удалить узлы), либо если узлы вырабатывают гормоны в излишних количествах и тем самым нарушают общий баланс гормонов (токсический зоб).
Все вышесказанное основано на еще одном положении.
Мы – клиника, которая доверяет результатам собственной тонкоигольной биопсии, потому что годы работы доказали нам самим – эндокринологам и хирургам-эндокринологам – что качество работы нашей цитологической службы находится на высоте. Именно поэтому мы и не оперируем всех подряд – у нас есть возможность отбирать для операции только тех пациентов, кому она действительно может спасти жизнь.
И последний, третий вопрос – почему мы рекомендуем не переделывать биопсию у Вас по месту жительства, а сразу приезжать в Санкт-Петербург?
За последние годы в 60% случаев консультация цитологических препаратов, доставленных к нам в центр из различных регионов России (от Калининграда до Камчатки и от Сочи до Мурманска), закончилась установлением другого диагноза. Только вдумайтесь в эту цифру – 60%! Можно долго демонстрировать здесь примеры диагностических ошибок – как в сторону установления несуществующего рака в доброкачественных узлах, так и в сторону пропуска явного рака – но вывод нам пришлось сделать один: необходимо самим иметь возможность сдать пациенту качественное УЗИ щитовидной железы, самим выбрать узлы, нуждающиеся в биопсии, самим эту биопсию провести и самим же изучить клеточный материал. Только в этом случае мы можем отвечать за качество биопсии в целом.
Фолликулярная аденома щитовидной железы — операция
Если же Вам потребуется в результате обследования по поводу диагноза «Фолликулярная аденома щитовидной железы» лечение
– мы можем гарантировать качество его проведения только в том случае, если все этапы – от подготовки к операции и предоперационного обследования до выписки из стационара и выдачи гистологического заключения – мы выполнили сами.
Кстати, если в результате обращения в нашу клинику с заключением «Фолликулярная аденома щитовидной железы» операция оказалась необходимой, и Вы решили госпитализироваться в наш центр – Вы проведете в клинике всего 2 суток (48 часов). В первый день Вы поступаете в клинику в 12 часов, после чего Вам проводятся необходимые обследования и осмотры анестезиолога, хирурга, терапевта; утром второго дня Вас оперируют, а утром третьего дня Вы уже покидаете клинику и можете отдохнуть в гостинице. Через 2 дня после выписки уже готово окончательное гистологическое заключение, по итогам которого Вас последний раз консультирует хирург-эндокринолог и дает Вам все необходимые советы – и Вы едете домой. Современные технологии и отработанная годами тактика лечения позволяет работать эффективно и быстро.
Ранняя выписка возможна потому, что мы практически никогда при операции не используем дренажи для выпуска остатков крови наружу, мы не пересекаем мышцы шеи и тем самым резко снижаем травматичность операции, а кожу после операции мы сшиваем косметическим швом рассасывающимися шовными материалами. На кожу накладывается специальный клей, который позволяет обходиться без повязки и дает возможность уже на следующий день принимать душ.
Объем операции в каждом случае определяется индивидуально. Подавляющему большинству пациентов необходимо удалить одну долю щитовидной железы – ту, в которой находится узел, однако есть и случаи, когда необходимо удаление всей щитовидной железы. Врачи нашего центра всегда помогут определиться в том, какой объем необходим именно Вам.
Годы работы показали, что наша работа нужна людям – за последние годы жителям практически всех регионов России проводилось повторное обследование в Санкт-Петербурге в связи с выявленным по месту жительства диагнозом «Фолликулярная опухоль щитовидной железы» + операция. Отзывы
наших пациентов – и тех, кому операция оказалась не нужна, и тех, кому ее все же пришлось провести – показывают нам, что пациенты в итоге довольны, что они приехали к нам.
Обследование и лечение проводятся платно или бесплатно?
Амбулаторное обследование (биопсия, анализы на гормоны и онкомаркеры, консультации врачей) проводятся платно, но цены мы стараемся поддерживать очень умеренные.
При необходимости операции на щитовидной железе жителям всех регионов России стационарное лечение проводится бесплатно, по системе федеральных квот либо по полису обязательного медицинского страхования. Бесплатно – означает бесплатно полностью
(включая пребывание в клинике, операцию, наркоз, необходимые обследования). Даже при бесплатном лечении в нашем центре Вам будет обеспечен высокий комфорт пребывания (комфортабельные 2-3-местные палаты с санузлом, кондиционером, ТВ, беспроводным интернетом, качественное питание, качественный уход), использование только импортных расходных материалов при операции и высококачественного наркоза, за который с Вас никто не будет требовать дополнительной оплаты.
Вы можете заказать дополнительные платные услуги в клинике только в том случае, если Вам потребуются какие-либо особые сервисные услуги (отдельная одноместная палата (при наличии), особый режим питания, выбор какого-либо определенного хирурга в качестве оперирующего врача).
Как приехать к Вам на консультацию и биопсию?
Для записи на биопсию и консультацию хирурга-эндокринолога или эндокринолога Северо-Западного центра эндокринологии Вам необходимо позвонить по телефону Петроградского или Приморского филиалов Центра эндокринологии:
- (812) 498-10-30, с 7.30 до 20.00, без выходных, Санкт-Петербург, Кронверкский пр., д. 31 (200 метров пешком налево от станции «Горьковская», в самом центре города, в 500 метрах от Петропавловской крепости). Для приезжающих на автомобилях есть парковка прямо перед входом в Центр.
- (812) 565-11-12, с 7.00 до 21.00 будни, с 7.00 до 19.00 — выходные, Санкт-Петербург, Савушкина ул., д.124, к.1 (250 метров направо от станции метро «Беговая»). Перед входом в Центр есть прилегающая парковка для автомобилей.
И напоследок…
Если Вам установлен по итогам тонкоигольной биопсии диагноз «Фолликулярная аденома щитовидной железы» — доверьте обследование, операцию и лечение в целом врачам, специализирующимся на этом заболевании. Только такой подход может обеспечить оптимальные результаты.
Мы ждем Вас!
-
Операция на щитовидной железе, медиальная тиреоидэктомия
Запись на операцию в Северо-Западный центр эндокринологии и эндокринной хирургии — ведущую специализированную клинику по лечению заболеваний щитовидной железы России и Европы: +7 812 980-77-21, +7 921 189-74-84, +7 921 420-30-31 (будни, с 9 до 17 часов). Мы принимаем на лечение пациентов из всех регионов России, стран ближнего и дальнего зарубежья.
-
Медуллярный рак щитовидной железы
Медуллярный рак щитовидной железы (медуллярная карцинома щитовидной железы) является редким гормонально активным новообразованием злокачественной природы, развивающимся из парафолликулярных клеток щитовидной железы
-
Удаление щитовидной железы
Информация об удалении щитовидной железы в Северо-Западном центре эндокринологии (показания, особенности проведения, последствия, как записаться на операцию)
-
Щитовидная железа. Заболевания щитовидной железы
В настоящее время изучению заболеваний щитовидной железы уделяется настолько серьезное внимание, что был выделен особый раздел эндокринологии — тиреоидология, т.е. наука о щитовидной железе. Врачей, занимающихся диагностикой и лечением заболеваний щитовидной железы, называют тиреоидологами.
-
Анализы в Санкт-Петербурге
Одним из важнейших этапов диагностического процесса является выполнение лабораторных анализов. Чаще всего пациентам приходится выполнять анализ крови и анализ мочи, однако нередко объектом лабораторного исследования являются и другие биологические материалы.
-
Анализ на гормоны щитовидной железы
Анализ крови на гормоны щитовидной железы — один из наиболее важных в практике работы Северо-Западного центра эндокринологии. В статье Вы найдете всю информацию, с которой необходимо ознакомиться пациентам, собирающимся сдать кровь на гормоны щитовидной железы
-
Консультация эндокринолога онлайн
Если вам необходимо получить консультацию эндокринолога, но возможности очно посетить специалиста нет, то оптимальным решением станет оформление дистанционной консультации.
-
Сделать биопсию
Для чего же необходимо проведение биопсии узлов щитовидной железы?
-
Операции на щитовидной железе
Северо-Западный центр эндокринологии – ведущее учреждение эндокринной хирургии России. В настоящее время в центре ежегодно выполняется более 5000 операций на щитовидной железе, околощитовидных (паращитовидных) железах, надпочечниках. По количеству операций Северо-Западный центр эндокринологии устойчиво занимает первое место в России и входит в тройку ведущих европейских клиник эндокринной хирургии
-
Консультация эндокринолога
Специалисты Северо-Западного центра эндокринологии проводят диагностику и лечение заболеваний органов эндокринной системы. Эндокринологи центра в своей работе базируются на рекомендациях Европейской ассоциации эндокринологов и Американской ассоциации клинических эндокринологов. Современные диагностические и лечебные технологии обеспечивают оптимальный результат лечения.
-
Тонкоигольная биопсия узлов щитовидной железы
Тонкоигольная биопсия — основной метод оценки морфологического строения узлов щитовидной железы. В ходе биопсии производится оценка клеточного состава узла, что дает возможность определения дальнейшей тактики лечения
-
Экспертное УЗИ щитовидной железы
УЗИ щитовидной железы является главным методом, позволяющим оценить строение этого органа. Благодаря своему поверхностному расположению, щитовидная железа легко доступна для проведения УЗИ. Современные ультразвуковые аппараты позволяют осматривать все отделы щитовидной железы, за исключением расположенных за грудиной или трахеей.
-
УЗИ шеи
Информация об УЗИ шеи — входящие в него исследования, их особенности
-
Консультация хирурга-эндокринолога
Хирург-эндокринолог – врач, специализирующийся на лечении заболеваний органов эндокринной системы, требующих использования хирургических методик (оперативного лечения, малоинвазивных вмешательств)
-
Интраоперационный нейромониторинг
Интраоперационный нейромониторинг — методика контроля электрической активности гортанных нервов, обеспечивающих подвижность голосовых связок, во время операции. При проведении мониторинга хирург имеет возможность каждую секунду оценивать состояние гортанных нервов и соответственно менять план операции. Нейромониторнг позволяет резко снизить вероятность развития нарушения голоса после операций на щитовидной железе и околощитовидных железах.
Биопсия — самый «близкий к телу» метод диагностики. От пациента отщипывают кусочек и изучают под микроскопом. В воображении некоторых пациентов биопсия приравнивается чуть ли не к хирургической операции. Это не так, хотя и то, и другое может проводиться одновременно. Что же такое биопсия, какая она бывает и для чего проводится, рассказывает MedAboutMe.
Что такое биопсия в медицине?
Биопсия — это метод анализа тканей человеческого организма. Суть его очень проста: взять образец органа (биоптат), извлечь его из организма и внимательно рассмотреть. Собственно, сам термин это и означает в переводе с греческого: bios — живой и opsis — наблюдение при помощи глаз, то есть, визуальное исследование живой ткани.
История биопсии начинается с имени арабского врача Альбукасиса, которого называют мусульманским отцом хирургии — он же Абу аль-Касим Аль-Захрави. Именно он впервые использовал полую иглу, чтобы получить образец тканей зоба щитовидной железы и впоследствии исследовать его. Долгое время врачи делали биопсию, скорее, случайно, чем намеренно. Но в конце XIX века все изменилось. Технологии исследования тканей при помощи микроскопа и возможности взятия образцов развились достаточно — и медицина получила новый метод.
В России первую диагностику при помощи биопсии провел в 1875 году доктор М.М. Руднев. В 1878 году немецкие ученые описали исследование образца шейки матки. А в 1879 году парижский дерматолог Эрнест Анри Бенье, который проводил научные изыскания в области болезней кожи, ввел термин «биопсия», обозначив им процедуру взятия образцов тканей.
Следует понимать, что биопсия — это инвазивный метод, то есть, при этом совершается проникновение в тело человека. И это травматичный метод, приводящий хоть и к минимальным, но повреждениям тканей. Поэтому врачи назначают биопсию тогда, когда без нее не обойтись. Просто так данный метод никогда не используется.
Итак, биопсия позволяет получить образец клеток или тканей. Его можно изучать на клеточном уровне, то есть, исследуется состояние отдельных клеток и их компонентов — цитологическое исследование, для которого может использоваться световой или более мощный, электронный микроскоп. А можно при помощи светового микроскопа анализировать срез ткани — при многих заболеваниях изменения происходят в структуре ткани органа. Иногда при проведении гистологического анализа требуется предварительная обработка образцов специальными растворами — их окрашивание или иная подготовка для диагностики.
В зависимости от того, какой метод предполагается использовать, биопсия проводится разными путями.
Как получить образец для исследования при биопсии?
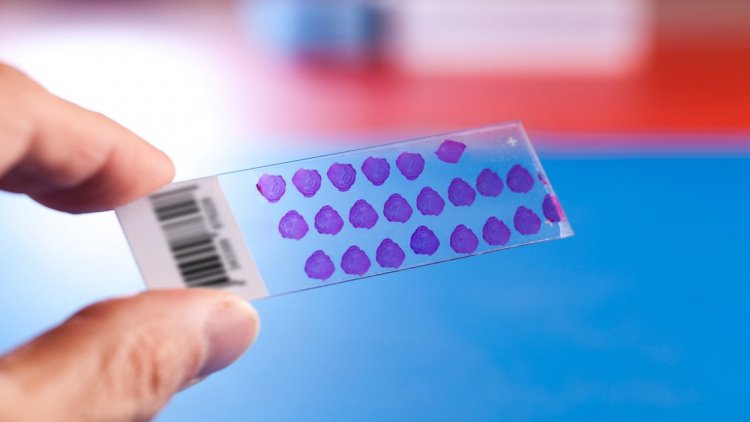
Для цитологического исследования образцы материала получают одним из следующих методов:
- Соскоб (мазок) — с пораженных тканей специальным шпателем или скальпелем на предметное стекло соскребается некоторое количество материала.
- Тонкоигольная биопсия — клетки органа или жидкость забираются путем отсасывания через полую длинную тонкую иглу. Так получают образцы костного мозга или кист.
При заборе кусочка тканей, в зависимости от того, какие ткани и каким образом надо исследовать, выделяют два вида биопсии:
- Эксцизионная — при этом удаляется и направляется на исследование все образование, а не отдельная его часть. Например, это может быть подозрительная родинка. В этом случае биопсия является одновременно и лечебной, и диагностической процедурой: сначала подозрительные ткани полностью удаляют, а потом проверяют: насколько они были опасны и не стоит ли поискать другие проявления болезни.
- Инцизионная — на исследование забирается только часть пораженной болезнью ткани.
Забор тканей может проводиться разными путями:
- Пункционная биопсия — образец тканей забирается при помощи полой иглы. Обычно используется для получения образца тканей, расположенных недалеко от поверхности кожи.
- Трепан-биопсия позволяет получать образец ткани в виде столбика при помощи трепана — специальной полой трубки. Используется при необходимости получения образца из плотных опухолей и костей.
- Кор-биопсия (режущая, сердцевинная биопсия) — разновидность трепан-биопсии, отличающаяся от нее механическими особенностями трепана. Проводится при помощи биопсийного пистолета — устройства для получения образцов молочной и щитовидной желез, почек, простаты, печени и других мягких тканей.
- Петлевая биопсия — при этом образец забирается при использовании петли и устройства, позволяющего резать ткань (коагулятор или радиочастотный аппарат). Проводят при эндоскопических исследованиях, а также при гинекологическом обследовании и др.
- Щипковая биопсия (панч-биопсия) — образец ткани удается получить при помощи специальных щипцов. Чаще всего используется при заболеваниях пищевод, желудка и кишечника.
- Скарификационная биопсия проводится устройством, позволяющим срезать тонкий слой ткани. Обычно используется при необходимости проведения биопсии кожи.
Самый частый побочный эффект биопсии — боль при проведении процедуры. Поэтому в большинстве случаев предварительно проводится местная анестезия — обезболивание конкретного участка, на котором будет проводиться забор тканей. Но, если речь идет только о соскобе, то, конечно, анестезия не нужна.
Биопсия не проводится при нарушениях свертываемости крови, а также при возможности получить требуемые данные другими, неинвазивными методами диагностики.
Биопсия и диагностика заболеваний
Устоялось мнение, что биопсия проводится, прежде всего, для опровержения или подтверждения предварительного диагноза «рак». И действительно, этот метод обязателен для окончательной постановки диагноза онкологами. Но он также успешно применяется и в других направлениях медицины, а не только в онкологии.
- Урологи исследуют ткани мочеполовой и мочевыделительных систем для поиска воспалительных процессов почек и мочевого пузыря, а также кистозных образований в них;
- Гинекологи при помощи биопсии диагностируют бесплодие, воспаление, предраковые состояния, а также некоторые эндокринные болезни;
- Гастроэнтерологи анализируют состояние желудочно-кишечного тракта: выявляют участки воспаления и ткани в предраковом состоянии и др.;
- Пункция лимфатических узлов проводится для их оценки при аутоиммунных, инфекционных и онкологических заболеваниях.
- Биопсия пересаженных органов необходима, чтобы проверить, не идет ли реакция отторжения.
- Пункция спермы может проводиться для оценки фертильности в ходе лечения бесплодия.
А в феврале этого года американские ученые сообщили, что разработали метод ранней диагностики болезни Паркинсона путем биопсии тканей подчелюстной слюнной железы. Метод позволяет выявить белок, указывающий на наличие болезни, на стадии, когда нет даже первых признаков заболевания. Это значит, что можно будет раньше начать лечение.
Обычно биопсия назначается, когда нет других возможностей получить информацию о клетках и тканях пораженного органа. Причем нередко забор тканей проводится «заодно» — раз уж все равно добрались до больного органа, почему бы не отщипнуть кусочек для анализа. То есть, взять образец тканей можно в процессе хирургической операции или других диагностических процедур, таких как:
- эндоскопия,
- колоноскопия,
- бронхоскопия и др.
Для проведения биопсии врач может воспользоваться дополнительным оборудованием, позволяющим наблюдать за процедурой, чтобы «не промахнуться» — томографом, аппаратом УЗИ или иной аппаратурой.
Ошибки при проведении биопсии

Идеальных методов диагностики медицина не знает. При проведении биопсии тоже возможны ошибки и получение ложноотрицательного результата, то есть, болезнь есть, но ее не нашли. Так, считается, что гистологическое исследование тканей — довольно точный метод и достоверен на 90%. Что может быть причиной ошибок при биопсии:
- при заборе было получено слишком мало материала и его оказалось недостаточно для полноценной диагностики;
- забор материала для анализа произведен не из опухоли, а из здоровых тканей рядом с ней;
- материал взят из зоны фиброза или некроза опухоли и не дает достаточно информации, чтобы определить наличие злокачественного образования;
- при подготовке материала к исследованию срез был проведен под неудачным углом;
- врач-морфолог не обладал достаточным опытом для выявления характерных признаков на сложном образце.
Выводы
- Биопсия — инвазивный, но малотравматичный метод диагностики, который никогда не назначается врачом просто так, без достаточных на то оснований. Если врач считает, что нужна биопсия — лучше не спорить, часто вовремя проведенный анализ является залогом жизни пациента.
- Современные технологии позволяют провести биопсию качественно и практически безболезненно.
- Результаты биопсии считаются окончательными. По ним врач может назначать лечение. Если результаты вызывают сомнения у врача (например, по всем признакам есть опухоль, а биопсия ее не показала) — возможна ошибка при заборе пробы. В этом случае врач может направить пациента на повторный анализ.
- Если результаты биопсии вызывают сомнения у пациента, он может забрать свои «стекла» с гистологическими срезами и отправить их на повторный анализ в другую клинику.
Клиническая лабораторная диагностика: национальное руководство / Под ред. В. В. Долгова, В. В. Меньшикова. – 2012
Руководство по лабораторным методам диагностики / Кишкун А.А. – 2013
Диагностика заболеваний редко обходится без инструментальных и лабораторных исследований. Оценки симптомов недостаточно — нужно узнать, что происходит внутри органов и тканей. Одним из наиболее точных методов обследования является биопсия. Врач производит забор тканевого материала в области предполагаемого патологического процесса с целью его дальнейшего изучения. Микроскопический анализ полученного образца помогает выявить характерные для определенного заболевания изменения. В онкологической практике биопсия считается информативным методом уточнения типа опухоли, ее стадирования.

- Что это за анализ?
- Показания к проведению
- Виды и способы проведения биопсии
- Подготовка
- Может ли биопсия быть ошибочной?
Что это за анализ?
Биопсия — высокоинформативный способ обследования, применяемый в случае необходимости анализа клеток в определенной анатомической области. Забор тканей с их последующим обследованием с помощью микроскопии дает возможность точно оценить клеточный состав. Без такой процедуры сложно обойтись, если врач подозревает наличие доброкачественного или злокачественного новообразования в определенном органе. Это уточняющее исследование, дополняющее результаты других диагностических процедур. Онколог анализирует результаты биопсии, рентгенографии, эндоскопии и иммунологических тестов совместно.
Онкологические заболевания развиваются быстро и угрожают жизни пациента. Нужно как можно раньше выбрать наиболее эффективную схему лечения. Именно с этой целью проводится биопсия. По результатам процедуры врач приходит к выводу, какие травматичные или даже опасные с точки зрения осложнений способы лечения уместны в данном случае. Подбирается тактика оперативного вмешательства, радиотерапии, химиотерапевтического лечения. Все это было бы невозможно без точного определения типа опухоли, ее стадии и распространенности в организме. Нужны цитологические и гистологические тесты.
В качестве примера можно привести злокачественное новообразование прямой кишки, растущее в нижней части органа. В качестве основного метода лечения выполняется иссечение этой анатомической структуры с последующим формированием колостомы для выделения каловых масс. Если диагноз не был полностью подтвержден, подобное вмешательство не проводят. Оно может по ошибке сделать пациента инвалидом.

Показания к проведению
Подобная диагностическая процедура требуется, если врач предполагает о наличии патологического процесса, подтверждение которого невозможно с помощью других способов исследования. В большинстве случаев это онкологические болезни, однако область применения биопсии ими не ограничивается. Например, такое исследование часто назначают гастроэнтерологи для оценки состояния слизистой оболочки органов пищеварительного тракта. Определяется вид воспалительного процесса, подбирается способ его лечения. В гинекологии и эндокринологии этот метод дает возможность определить причину нарушения фертильности, обнаружить ранние признаки воспаления и дисплазии.
Также биопсия необходима для определения особенностей течения и степени тяжести патологического процесса при болезнях печеночной ткани, почек, головного мозга, мышц и других анатомических структур. Это важно для подбора и изменения схемы медикаментозной терапии. По результатам анализа врач определяет прогностические данные.
Виды и способы проведения биопсии
В современной клинической практике чаще всего используют следующие методики выполнения биопсии:
- Мазки, соскобы и бритвенный метод. Зачастую специалисту требуется небольшое количество материала для постановки диагноза. Можно выполнить мазок и получить все необходимые данные при его последующей микроскопии. Например, такой способ часто применяют в гинекологии. Бритвенная биопсия предполагает иссечение тонкого участка кожного покрова с помощью скальпеля или другого инструмента.
- Тонкоигольная пункция. Такая процедура тоже подходит для случаев, когда достаточно получить немного клеток. В область предполагаемого патологического процесса вводится тонкая игла, захватывающая тканевой образец.
- Толстоигольная пункция. Позволяет произвести забор большого образца тканей без иссечения. Ее назначают при злокачественном новообразовании молочной железы, печеночной ткани, предстательной железы. Трепан-биопсия подходит для исследования кожного покрова, костномозговых структур. Используется специальный инструмент в форме цилиндра.
- Аспирационный метод. Это современная техника забора материала, при котором используется вакуумный прибор в форме цилиндра. В качестве механизма применяется отрицательное давление. Прибор присоединяют к игле. Аспирация дает возможность взять несколько образцов в разных участках анатомической структуры.
- Операционная биопсия. Проводится непосредственно во время операции, когда врач иссекает опухолевую ткань. Это высокоинформативное исследование, позволяющее оценить состояние большого количества тканей. Минус такого вида процедуры — определить тип болезни можно только после операции. Плюсом можно считать совмещение лечебной практики с достоверной диагностикой.
- Эндоскопическая биопсия. Проводится во время диагностики внутренних полостных структур, вроде пищеварительного или респираторного тракта. С помощью эндоскопа врач осматривает подозрительные участки тканей и выбирает место забора материала. Плюсом такой техники можно считать повышенную точность результатов исследования.
Способ проведения диагностики выбирают в зависимости от анамнеза пациента.

Подготовка
В большинстве случаев специально готовиться не следует. Достаточно прийти к врачу в день проведения процедуры и подписать необходимые документы. Специалист объяснит, как будет проходить обследование. Расскажет о рисках и возможных неприятных ощущениях. Определенные виды биопсии выполняют под местным обезболиванием. Реже требуется наркоз. Пациент может сам выбирать комфортный для него способ выполнения диагностики. В случае наркоза нужны специальные подготовительные процедуры.
Для биопсии характерны стандартные осложнения, возникающие при других видах вмешательств. Возможно кровоизлияние, инфицирование тканей. Реже возникает травматизация внутренних органов. Такие негативные последствия редки, но врач обязательно уведомляет пациента о рисках.

Может ли биопсия быть ошибочной?
Достоверность исследования зависит от способа его проведения, анамнеза пациента, опыта врача и других факторов. Например, при пункции специалист может получить образец тканей без злокачественных клеток, если игла попала в соседнюю с опухолью область. В этом случае возможен ложноположительный результат. Онкологи учитывают такую вероятность, и всегда назначают уточняющие исследования. Диагноз не ставится только на основе результатов одной процедуры. Всегда проводится комплексная оценка состояния организма.

Пункция щитовидной железы — процедура, во время которой в железу вводят иглу, чтобы получить образец ткани для исследования. Данная манипуляция называется тонкоигольной аспирационной биопсией. Ее проводят, когда в щитовидной железе обнаруживают узел, как правило, чтобы разобраться, является ли он злокачественным.

Наш эксперт в этой сфере:

Сергеев Пётр Сергеевич
Заместитель главного врача по лечебной работе. Врач-онколог, хирург, химиотерапевт, к.м.н.
Щитовидная железа — небольшой эндокринный орган, который находится под кожей на передней поверхности шеи. Она имеет форму буквы «Н» или бабочки, состоит из двух долей, соединенных узким перешейком. Щитовидная железа весит всего 12–25 г, ее объем составляет до 25 мл у мужчин и до 18 мл у женщин. Она накапливает йод и вырабатывает гормоны, которые влияют на многие процессы в организме, участвуют в регуляции обмена веществ, роста отдельных клеток и организма в целом.
У некоторых людей в щитовидной железе возникают уплотнения — узелки. Чаще всего это доброкачественное разрастание нормальной ткани, киста, проявление хронического воспаления, многоузлового зоба, эндемического зоба, связанного с недостатком йода. Злокачественными являются менее 5% всех узелков, обнаруживаемых в щитовидной железе. В ряде случаев установить точный диагноз можно только после биопсии.
Тонкоигольная аспирационная биопсия щитовидной железы — безопасный и информативный метод диагностики, который обладает многими преимуществами:
- Высокая точность диагностики — 95%.
- Надежность: в большинстве случаев можно достоверно судить о том, является ли узел в щитовидной железе доброкачественным или злокачественным.
- Чтобы получить образец ткани, не нужно делать разрез и применять общую анестезию.
- При применении местной анестезии процедура является совершенно безболезненной.
- Короткий восстановительный период.
В каких случаях необходима пункция щитовидной железы?
Обычно узлы в щитовидной железе выявляет врач-эндокринолог во время пальпации (ощупывания), либо их обнаруживают в ходе УЗИ. Иногда встречаются большие узлы, которые заметны под кожей, деформируют шею, нарушают дыхание и глотание.
Некоторым пациентам достаточно пройти ультразвуковое исследование, компьютерную томографию шеи и сдать анализ крови на гормоны. Эти методы диагностики могут показать, что узел не является злокачественным. Но в большинстве случаев диагноз приходится уточнять с помощью пункции и тонкоигольной биопсии.
Заподозрить злокачественный характер узла во время УЗИ можно по некоторым признакам:
- низкая эхогенность (темный цвет на снимках);
- неоднородная структура;
- отсутствие вокруг узла темного ободка Хало — обычно он выявляется при доброкачественных образованиях;
- неровные, нечеткие границы;
- неправильная форма;
- наличие уплотнений — кальцинатов;
- обильное или, напротив, скудное кровоснабжение;
- увеличение лимфатических узлов — это может говорить о том, что они тоже поражены злокачественной опухолью.
Риск того, что узел окажется злокачественным, повышен у людей с отягощенным семейным анамнезом (рак щитовидной железы у близких родственников), у тех, кто ранее страдал раком эндокринных органов, подвергался воздействию ионизирующих излучений.
В соответствии с современными рекомендациями, диагностическая пункция показана, когда в щитовидной железе обнаружен узел диаметром 1 см и более, который определяется на ощупь.
Врач принимает решение о том, нужно ли проводить пункцию щитовидной железы и биопсию узла, в каждом случае индивидуально, изучив результаты УЗИ и других исследований. Некоторые критерии играют важную роль:
| Факторы, которые свидетельствуют о высоком риске рака щитовидной железы | Факторы, которые указывают на низкий риск злокачественной опухоли (пункцию можно отложить) |
|
|
Вы можете получить консультацию у компетентного специалиста в международной клинике Медика24. Наши врачи работают в соответствии с современными международными стандартами.
Закажите обратный звонок. Мы работаем круглосуточно
Записаться на прием

Сообщение отправлено!
ожидайте звонка, мы свяжемся с вами в ближайшее время
Подготовка к процедуре
Пункция щитовидной железы не требует специальной подготовки. Не нужно корректировать образ жизни, придерживаться специальной диеты и пр. Если пациент постоянно принимает какие-либо лекарства, то их не нужно отменять, за исключением антикоагулянтов. Эти препараты применяются для «разжижения крови» и предотвращения образования тромбов. Из-за них после пункции щитовидной железы может повыситься риск кровотечения. Стоит ли их отменить за несколько дней до процедуры, решает врач.
Обычно тонкоигольную аспирационную биопсию выполняют врачи-эндокринологи. У них это получается лучше, чем у других специалистов, потому что им часто приходится заниматься пальпацией щитовидной железы. Желательно, чтобы пункцию проводил врач, который будет в дальнейшем вести пациента.
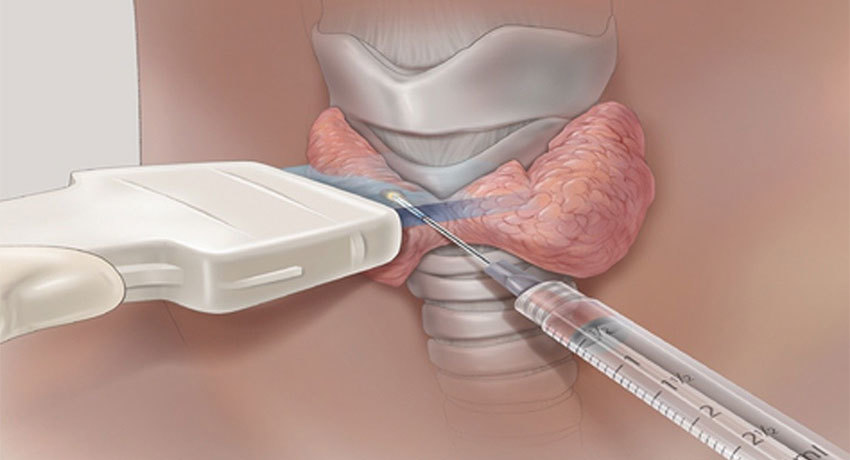
Как проводится пункция?
Диагностическая пункция щитовидной железы в среднем продолжается 20 минут. Во время процедуры пациента обычно укладывают на спину и подкладывают под плечи подушку, чтобы немного запрокинуть голову. Это упрощает доступ к щитовидной железе для врача.
Общий наркоз во время пункции не нужен. Некоторые врачи используют местную анестезию — обкалывают область вмешательства раствором лидокаина. Это позволяет полностью избежать болевых ощущений. Анестезию можно и не проводить. В таком случае ощущения во время пункции будут такими же, как во время укола в вену.
Для аспирационной биопсии используют тонкую иглу (22, 25 или 27 калибра) и шприц объемом 10–20 мл. Для удобства его можно вставить в специальный металлический держатель.
Пункцию щитовидной железы проводят под контролем ультразвука. УЗ-навигация помогает ввести иглу точно в нужное место и не повредить соседние анатомические структуры.
Рекомендуется получить образцы ткани не менее чем из 2 мест — за счет этого снижается риск ошибки. Зачастую делается 3–6 попыток, а некоторые эксперты рекомендуют не менее шести.
Если в щитовидной железе имеется киста (полость с жидкостью), то в нее вводят иглу, аспирируют содержимое, а затем проводят биопсию оставшейся ткани. Жидкость из кисты собирают в отдельную емкость и отправляют на цитологическое исследование.
После процедуры
После того как получены необходимые образцы ткани, иглу извлекают и к месту прокола прикладывают тампон, осуществляя им давление. Когда кровь останавливается, наклеивают пластырь. Его можно снять через несколько часов. Пациента просят медленно сесть, чтобы у него не закружилась голова. За его состоянием наблюдают несколько минут, а затем отпускают в палату или домой.
В течение 1–2 дней в месте пункции могут беспокоить боли. С ними можно справиться с помощью обезболивающих препаратов и холода местно.
Возможные осложнения
Пункция щитовидной железы редко сопровождается осложнениями. Навигация с помощью ультразвука делает эту процедуру еще более безопасной. Случаи распространения злокачественной опухоли из-за введения иглы, повреждения соседних органов, нервов, кровеносных сосудов практически не встречаются.
Чаще всего после тонкоигольной биопсии беспокоят боли и немного меняется цвет кожи в месте укола. Но даже небольшие кровоизлияния на коже — редкость. Описаны единичные случаи, когда развивалось кровотечение в кисту, и
из-за
этого ее приходилось удалять.
Если соблюдаются правила асептики и антисептики, риск инфицирования также крайне маловероятен.

Сообщение отправлено!
ожидайте звонка, мы свяжемся с вами в ближайшее время
Возможны ли ошибки?
Аспирационная биопсия щитовидной железы — довольно точный метод диагностики. Тем не менее, в редких случаях могут происходить ошибки:
- Ложноположительный результат — когда злокачественной опухоли нет, а специалисты лаборатории посчитали, что она есть. Вероятность такой ошибки составляет 3%.
- Ложноотрицательные результаты встречаются менее чем в 5% случаев. При этом в лаборатории не обнаруживают опухолевые клетки, а на самом деле у пациента имеется злокачественная опухоль.
Причины ошибок бывают разными: неопытность врача, который выполнял пункцию, сотрудника лаборатории, особенности гистологического строения разных новообразований. В узелки диаметром менее 1 см бывает сложно попасть иглой, а при размерах более 4 см не удается собрать образцы ткани из всех частей узла.
Если у вашего лечащего врача есть сомнения в диагнозе — получите услугу второго врачебного мнения у специалистов в международной клинике Медика24.
Чего ожидать после того, как придет заключение из лаборатории?
В патоморфологической лаборатории образцы ткани, полученные во время пункции щитовидной железы, изучают под микроскопом, проводят различные исследования, чтобы оценить характеристики клеток.
Спустя несколько дней из лаборатории приходит заключение, в котором указан патоморфологический диагноз:
- «Доброкачественное образование» — такой вердикт выносят по результатам примерно 70% биопсий щитовидной железы. Чаще всего дальнейшего лечения не требуется, узлы нужно контролировать с помощью УЗИ каждые 18 месяцев. У 3% из этих пациентов в дальнейшем обнаруживают злокачественные опухоли.
- «Злокачественное новообразование». Опухолевые клетки находят в 3–7% биоптатов. Точность диагноза составляет 97–99%. У 1–3% пациентов на самом деле нет рака.
- «Подозрение на злокачественное новообразование». Вероятность того, что в данном случае имеется злокачественная опухоль, составляет 60–75%. Обычно таким пациентам назначают хирургическое лечение.
- «Атипия неопределенного значения» (AUS) или «фолликулярное изменение неопределенного значения» (FLUS) — если коротко, то эти термины означают, что в целом клетки выглядят нормальными, но есть некоторые признаки, вызывающие беспокойство. Риск рака у таких пациентов составляет 5–15%. В таком случае врач может назначить повторную биопсию или генетический анализ.
- «Фолликулярное новообразование» или «подозрение на фолликулярное новообразование» — еще один неопределенный патоморфологический диагноз. Риск рака составляет 15–30%. Ситуацию может прояснить генетический анализ. Врач может назначить удаление пораженной половины щитовидной железы — гемитиреоидэктомию, с последующим гистологическим исследованием.
- «Недостаточно клеток для диагностики» — к сожалению, такие ситуации иногда тоже встречаются. Необходима повторная биопсия.
Обратитесь в международную клинику Медика24: наши врачи обладают большим опытом проведения аспирационной тонкоигольной биопсии щитовидной железы. Исследования биоптатов проводятся в современной лаборатории, оснащенной новейшей аппаратурой. Это позволяет существенно повысить эффективность диагностики и свести к минимуму вероятность ошибки. Если онкологический диагноз подтвердится — в нашей клинике можно сразу начать комплексное лечение в соответствии с современными международными рекомендациями.
Материал подготовлен членом международного общества хирургов онкологов EESG, кандидатом медицинских наук Сергеевым Петром Сергеевичем.

Содержание:
- Показания и противопоказания к пункции щитовидной железы
- Подготовка и техника проведения пункции щитовидной железы
- Лабораторный этап исследования и его результаты
- Варианты заключений цитолога
Патология щитовидной железы довольно распространена, особенно, в некоторых географических зонах, а по данным статистики, к 50-летию примерно половина женского населения планеты «обзаводится» узлами в органе. С увеличением возраста растет и этот показатель, и к 70 годам узлы можно обнаружить практически у всех. Такая ситуация требует от врачей не только своевременной диагностики патологического процесса и исключения рака, но и дифференцированного подхода в отношении необходимости операции.
Пункция щитовидной железы с последующим цитологическим исследованием ее ткани считается едва ли не самым важным методом диагностики заболеваний органа. Раньше основное значение имело УЗИ, однако оно не дает абсолютной точности, возможны ошибочные выводы и, соответственно, неправильная тактика ведения, поэтому тонкоигольная биопсия под контролем УЗИ — «золотой стандарт» при обследовании больных, имеющих ту или иную патологию.
Результат пункции диктует врачу дальнейшую тактику ведения пациента — оперировать, наблюдать или лечить консервативно, ведь не зная точно, какое строение имеет образование в паренхиме органа, эндокринолог рискует ошибиться, а последствия окажутся плачевными для больного.
Многие считают, что раз назначена пункция, то впереди обязательно ждет и операция. Однако это не совсем так. Действительно, еще совсем недавно хирурги придерживались активной тактики для большинства пациентов с узлами в органе, но появление высокоинформативных способов диагностики и исключения рака позволило значительно снизить число необоснованно прооперированных.
Учитывая данные статистики относительно распространенности узлообразования в щитовидной железе и проводя всем без исключения удаление и узлов, и органа, хирурги оставили бы без щитовидной железы практически всех людей пожилого возраста. Понятно, что оправданным такой подход считать нельзя, ведь операция имеет ряд осложнений — нарушение голоса, расстройства кальциевого обмена и т. д. Кроме того, хирургия — это еще и весьма затратная сфера в системе здравоохранения, и чем больше операций проводится необоснованно, тем выше и бесполезные траты бюджетных средств.
Таким образом, пункция щитовидной железы позволяет ответить на несколько важнейших вопросов: злокачественный или доброкачественный характер несет в себе узел щитовидной железы, есть ли показания к оперативному лечению, каков должен быть его объем.
Применение пункции показало, что лишь около 5% всех узловых образований щитовидной железы являются злокачественными, остальные — «добрые», не имеющие склонности малигнизироваться. Точное определение показаний к операции снизило число прооперированных больных почти в десять раз, но среди тех, кому удалили орган, значительно возросло количество случаев рака. Это говорит о том, что операции после внедрения пункционной биопсии стали проводиться тем, кому они действительно нужны.
Роль пункционной биопсии в диагностике патологии щитовидной железы сложно переоценить. Благодаря своей информативности, метод успешно применяется во всех эндокринологических клиниках, он прост в исполнении, не требует дорогостоящего оснащения и хорошо переносится большинством пациентов.
Показания и противопоказания к пункции щитовидной железы

Если ранее считалось, что проведение пункционной биопсии показано всем пациентам с наличием узла в щитовидной железе более 1 см в диаметре, то в настоящее время показания к ее проведению многими профильными организациями во всем мире ограничиваются. Так в России с недавних пор применяется система сонографической оценки стратификации риска злокачественности узлового образования щитовидной железы EU TIRADS, согласно которой для определения показаний к проведению биопсии учитывается сонографическая структура и размеры узлового образования.
Алгоритм EU-TIRADS для стратификации риска злокачественных новообразований и принятия решения о ТАБ.

Согласно системе EU TIRADS пункционная биопсия узлов, которые являются со 100% вероятностью доброкачественными (простые кисты и губчатые (спонгиформные) узлы) можно не пунктировать.


Узлы, которые согласно системе EU-TIRADS имеют низкий риск злокачественности (EU-TIRADS-III) – 2-4% (овальные, с ровным краем, изоэхогенные/гиперэхогенные солидные узлы) подлежат пункционной биопсии при размере узла более 2 см в диаметре.


Узлы, имеющие средний (промежуточный) риск злокачественности (овальные, с ровным краем, слегка гипоэхогенные узлы) (EU-TIRADS IV) – 6-17%, необходимо пунктировать при размерах более 1,5 см в диаметре.

А вот узлы, имеющие высокий риск злокачественности (EU-TIRADS V) подлежат пункционной биопсии при размере 1 см в диаметре. К таким узлам относятся узловые образования, имеющие хотя бы один из больших признаков злокачественности:
- неправильная форма
- неровный край
- микрокальцинаты
- выраженная (по отношению к претиреоидным мышцам) гипоэхогенность
Риск злокачественности таких узлов составляет 26-87%!




Как правило, такие узлы лучше пропунктировать из 2-3 точек.
Повторная биопсия может быть показана в случае, когда первоначально доброкачественный процесс начинает вести себя подозрительно в отношении рака — появляется бугристость контуров, в паренхиме на УЗИ видны кальцинаты, а на шее прощупываются увеличенные лимфатические узлы.
Также пациенту могут назначить повторное исследование, если первая биопсия была проведена не в специализированном медицинском центре либо при исследовании были допущены ошибки, неточность в формулировках, материал оказался неинформативным и т. д.
Противопоказаний к тонкоигольной пункционной биопсии щитовидной железы практически нет. Метод считается безопасным для абсолютного большинства больных. Однако сложности могут возникнуть при обследовании детей младшего возраста, лиц с психическими отклонениями, которым может быть показан кратковременный общий наркоз на время исследования. В случае гипертонических кризов, аритмий и других сердечно-сосудистых нарушений вопрос о безопасности и времени проведения процедуры решается индивидуально.
Подготовка и техника проведения пункции щитовидной железы
Забор биопсийного материала из щитовидной железы проводится амбулаторно и занимает около четверти часа. Большая часть времени уходит на укладывание пациента, оформление документации, объяснение сути манипуляции, в то время как сам прокол и получение ткани — это считанные минуты.
 Какой-либо специальной подготовки перед пункцией не требуется. Больной может вести привычный образ жизни, пить и есть накануне исследования. Принимаемая пища не окажет влияния на результат, узел не изменит от нее своего строения, однако чувствительные и эмоциональные люди могут испытывать тошноту, головокружения и даже падать в обморок, поэтому лучше все же на нагружать свой желудок чрезмерно, но и отказываться от еды недопустимо, ведь обморок может наступить и у проголодавшихся пациентов.
Какой-либо специальной подготовки перед пункцией не требуется. Больной может вести привычный образ жизни, пить и есть накануне исследования. Принимаемая пища не окажет влияния на результат, узел не изменит от нее своего строения, однако чувствительные и эмоциональные люди могут испытывать тошноту, головокружения и даже падать в обморок, поэтому лучше все же на нагружать свой желудок чрезмерно, но и отказываться от еды недопустимо, ведь обморок может наступить и у проголодавшихся пациентов.
Немаловажно подготовиться к процедуре и психологически, ведь излишний страх не только не оправдан, но и мешает самому пациенту объективно оценивать свое самочувствие. Возможная боль — основная причина страха. Учитывая, что укол производится в шею, он еще больше усиливается.
Многие пациенты боятся пункции и начинают паниковать заранее, думая, что это больно и крайне неприятно, а в последствии их непременно ждет операция. Однако, им можно успокоиться: применение тонких игл и, при необходимости, местных анестетиков делает пункцию почти безболезненной. Ощущения от нее сродни тем, которые все мы испытывали не раз при внутримышечных инъекциях, то есть вполне терпимы.
Другим поводом для беспокойства может стать опасение, что хирург попадет иглой не туда, куда нужно, либо спровоцирует прогрессирование патологии. Об этом не стоит беспокоиться, учитывая, что все пункции проводятся под контролем ультразвукового датчика, а после процедуры не происходит ускорения роста узлов или распространения опухоли за пределы органа.
Современные стандарты пункции щитовидной железы требует проведения процедуры только под контролем УЗИ. Дополнительная визуализация органа и объемных образований в нем повышает точность прокола до 100%, исключает взятие ткани из другого участка, позволяет сделать пункцию в наиболее измененной области узла.
Большинство больных не нуждаются в анестезии, поскольку прокол осуществляется крайне быстро, и тонкая игла практически не травмирует железу. Показания к операции зависят от результата цитологии, и необходима она далеко не каждому.
Особо чувствительным и эмоциональным субъектам может быть проведено местное обезболивание специальными кремами или спреями с анестетиком, что не снижает эффективности процедуры, но облегчает ее проведение для конкретного обследуемого.
Берут пункцию при помощи тонких игл, и чем меньше ее диаметр, тем лучше: больной меньше ощущает момент прокола, а врач получает более качественный материал, не смешанный с кровью в связи с малой травматичностью.
 Пункция узла щитовидной железы проводится в процедурном кабинете и всегда под контролем ультразвука. Она включает несколько этапов:
Пункция узла щитовидной железы проводится в процедурном кабинете и всегда под контролем ультразвука. Она включает несколько этапов:
- Укладывание обследуемого на спину, под которую помещается валик или подушка, помогающая достичь максимального разгибания шейного отдела и облегчения доступа к железе;
- Поиск с помощью ультразвука узлового образования в паренхиме органа, уточнение его локализации и размеров, наличия дополнительных включений (кальцинаты, рубцы, кисты);
- Обработка кожи в месте прокола антисептическими средствами, ограничение зоны манипуляции стерильными салфетками;
- Введение пункционной иглы быстрым, но аккуратным движением в требуемую область под контролем УЗИ, забор материала для исследования;
- Извлечение иглы наружу и помещение полученной ткани на предметное стекло, которое после будет подвергнуто микроскопии.
Когда игла достигла узлового образования, хирург четко видит ее на экране аппарата УЗИ, продвигая в самый подозрительный участок патологического очага. По мере всасывания шприцем ткани хирург перемещает иглу в разных направлениях, стремясь изъять из органа как можно более разнообразный клеточный субстрат.
Цитологический мазок, полученный на предметном стекле, направляется на исследование к врачам-цитологам, которые помогут с определением окончательного диагноза. Заключение пациент получит в течение недели после исследования, в зависимости от сложности клинического случая и загруженности цитологической лаборатории.
Место прокола после извлечения иглы заклеивается лейкопластырем, и уже через 10-15 минут в случае хорошего самочувствия пациент может отправиться по своим делам. В день процедуры разрешается принимать душ, заниматься спортом, есть и пить в привычном режиме.
Пункция щитовидной железы считается безопасной и практически безболезненной процедурой и, вместе с тем, высокоинформативным и незаменимым этапом диагностического поиска. Осложнения при ней крайне редки, хотя исключить их полностью все же нельзя. Наиболее вероятными последствиями могут стать небольшая гематома в месте прокола кожи, что не представляет угрозы здоровью обследуемого, а также обмороки в момент забора ткани, которые более часты у эмоционально лабильных и чрезмерно боящихся исследования пациентов.
Лабораторный этап исследования и его результаты
Все пациенты, прошедшие пункцию щитовидной железы, хотят получить не только быстрый, но и максимально точный цитологический диагноз. Этого же желают и врачи, однако на деле случается иначе. Заключения могут быть не информативными, если в материале не было клеток, а содержался коллоид, если обнаружены признаки аутоиммунного тиреоидита, но ничего не сказано о характере опухолевидного образования и т. д.
Как показывает практика, вероятность получения точного цитологического ответа прямо связана с опытом хирурга, проводившего пункцию. Чем прицельнее он взял ткань для исследования, тем выше вероятность достоверного и развернутого вывода о характере патологии. Считается, что доля неинформативных ответов минимальна у специалиста, который проводит не менее 40 биопсий в неделю, а в крупных эндокринологических центрах этот показатель достигает нескольких сотен.
 Для повышения информативности и предупреждения повторных пункций в настоящее время проводится исследование пунктата из узла щитовидной железы методом жидкостной цитологии. В этом случае пунктат помещается не на предметное стекло, а в специальную емкость с жидкостью (виал). Далее, путем центрифугирования этой жидкости, происходит отделение клеток щитовидной железы от клеток крови и коллоида. В результате этого цитолог может более точно определиться с природой узлового образования щитовидной железы.
Для повышения информативности и предупреждения повторных пункций в настоящее время проводится исследование пунктата из узла щитовидной железы методом жидкостной цитологии. В этом случае пунктат помещается не на предметное стекло, а в специальную емкость с жидкостью (виал). Далее, путем центрифугирования этой жидкости, происходит отделение клеток щитовидной железы от клеток крови и коллоида. В результате этого цитолог может более точно определиться с природой узлового образования щитовидной железы.
Когда пациент уже покинул клинику, начинается наиболее сложный и ответственный этап всей морфологической диагностики. Стекла с мазками ткани железы просушиваются и отправляются в цитологическую лабораторию, где производится их окрашивание методиками Май-Грюнвальд-Гимзы или Папаниколау. Клетки исследуются микроскопически врачом-цитологом.
Морфологические особенности пунктата — строение клеток, их размеры, включения в цитоплазме, атипия — предопределяют диагноз, который в дальнейшем будет решающим при выборе лечебной тактики.
У 9 из 10 пациентов цитолог может сформулировать предельно точный диагноз, но случается, что данных микроскопии недостаточно для исключения или подтверждения злокачественности опухолеподобного процесса (много крови в пунктате, низкая клеточность ввиду плотности узла и др.).
Причиной неинформативности могут стать не только техническая погрешность при проведении процедуры или недостаточный опыт хирурга, но и слишком разнообразный клеточный состав, когда даже очень грамотному цитологу сложно выделить преобладающий тип клеток. В этом случае специалисту ничего не остается, как констатировать неинформативность материала и порекомендовать повторную пункцию железы.
В ожидании результатов исследования, пациенты очень волнуются, ведь главная задача хирурга и цитолога — исключить злокачественную опухоль. В среднем время ожидания результата занимает около недели, хотя само приготовление препаратов и их просмотр возможны в течение одного дня.
Крупные центры, специализирующиеся на патологии щитовидной железы, выдают заключения через 1-2 дня, так как штат специалистов позволяет провести диагностику максимально быстро даже при высокой загруженности пациентами. Это позволяет минимизировать стресс у больных в ожидании ответа без ущерба качеству исследования.
Пациенту на руки выдается заключение с результатом исследования, в котором указана не только цитологическая картина (главная цель пункции), но и точные размеры и расположение узлов, их особенности по данным ультразвукового осмотра. С этим документом обследуемый направляется к своему лечащему врачу-эндокринологу для решения вопроса о дальнейшей тактике. Если показана операция, то будет назначен оптимальный для нее срок, в противном случае пациент либо будет наблюдаться, периодически проходя УЗ-контроль, либо врач выпишет консервативное медикаментозное лечение.
 Варианты заключений цитолога
Варианты заключений цитолога
Для формулировки заключений цитологи всего мира используют единые международные рекомендации. Эти рекомендации требуют от специалиста максимально точного и краткого заключения, которое даст возможность хирургу или эндокринологу определить единственно верную тактику лечения.
Чтобы устранить значительную изменчивость в сообщениях о цитологических заключениях пункционной биопсии узловых образований щитовидной железы под эгидой Национального Института рака США в 2007 году были представлены согласованные рекомендации, известные как Bethesda System for Reporting Thyroid Cytopathology. Согласно системе Bethesda на основании результата цитологического исследования определяется тактика дальнейшего ведения пациента.
В России также цитологи описывают полученный при пункционной биопсии результат согласно этой системе.
Система цитологических заключений щитовидной железы Bethesda: категории диагностики и риск злокачественности
| Диагностическая категория | Расчетный/
прогнозируемый риск злокачественности |
|
| Bethesda I | Недиагностический / неудовлетворительный Nondiagnostic or unsatisfactory | 1–4 % |
| Bethesda II | Доброкачественный
Benign |
0–3 % |
| Bethesda III | Атипия неопределенного значения / фолликулярное поражение неопределенного значения
Atypia of undetermined significance or follicular lesion of undetermined significance (AUS / FLUS) |
5–15 % |
| Bethesda IV | Фолликулярное новообразование / подозрительное на фолликулярное новообразование
Follicular neoplasm or suspicious for a follicular neoplasm (FN / SFN) |
15–30 % |
| Bethesda V | Подозрительные на злокачественность
Suspicious for malignancy (SUSP) |
60–75 % |
| Bethesda VI | Злокачественная опухоль
Malignan |
97–99 % |
Рекомендации по использованию системы Bethesda Российской ассоциации эндокринологов (2016)
| — неинформативная пункция – вероятность злокачественности – 1 – 4%, рекомендуется повторная ТАБ; |
— доброкачественное образование – вероятность злокачественности – 0 – 4%, рекомендуется динамическое наблюдение. Показания к оперативному лечению при доброкачественном заключении ТАБ:
|
| — атипия неопределенного значения – вероятность злокачественности – 5 – 15%, рекомендуется повторная ТАБ; |
| —атипия неопределенного значения повторно – вероятность злокачественности – 20 –40%, рекомендуется гемитиреоидэктомия с интраоперационным гистологическим исследованием; |
| — фолликулярная неоплазия – вероятность злокачественности – 15 – 30%, рекомендуется гемитиреоидэктомия с интраоперационным гистологическим исследованием; |
| — фолликулярная неоплазия более 5 см – вероятность злокачественности более 50%, в связи с низкой чувствительностью интраоперационного гистологического исследования и высокой вероятностью повторной операции, возможно обсуждение с пациентом целесообразности выполнения тиреоидэктомии; |
| — подозрение на злокачественную опухоль – вероятность злокачественности – 60 – 75%, рекомендуется тиреоидэктомия; |
| — злокачественная опухоль – вероятность злокачественности – 97 – 99%, рекомендуется тиреоидэктомия. |
Рекомендации по использованию системы Bethesda Американской тиреоидологической ассоциации (American Thyroid Association — ATA) (2015)
| Диагностическая категория | Риск злокач. | Тактика |
| Bethesda I | 1-4% | Следует повторить ТАБ, — если возможно с цитологической оценкой на месте.
Если повторная ТАБ недиагностическая, узлы без сонографической картины высокого риска злокачественности требуют тщательного наблюдения. Хирургическое вмешательство следует рассматривать если узел имеет сонографическую картину высокого риска злокачественности, рост узла (> 20% в двух измерениях) или при наличии клинических факторы риска для злокачественного образования. |
| Bethesda II | 0-3% | Узлы с сонографической картиной высокого риска злокачественности – повторить УЗИ и ТАБ в течение 12 месяцев.
Узлы с сонографической картиной низкого и среднего риска злокачественности — повторить УЗИ через 12–24 месяца. Узлы с сонографической картиной очень низкого злокачественности (включая губчатые узлы) -наблюдение. Повторное УЗИ не ранее чем через 24 месяца. Если при повторной ТАБ получен доброкачественный результат наблюдение за узлами для подтверждения риска злокачественности не требуется. |
| Bethesda III | 5-15% | Для узлов с сонографической картиной высокого риска злокачественности – повторная ТАБ или молекулярное тестирование.
Если повторное цитологическое исследование, молекулярное тестирование или и то и другое не выполняются или не дают результатов, может быть выбрано либо наблюдение, либо диагностическая гемитиреоидэктомия в зависимости от клинических факторов риска, сонографических признаков или желания пациента. |
| Bethesda IV | 15-30% | Диагностическое хирургическое иссечение узла ЩЖ – гемитиреоидэктомия.
Тем не менее, возможно отложить оперативное лечение после рассмотрения клинических и сонографических особенностей узла, молекулярного тестирования. Информирование пациента и его мнение должны учитываться для принятия решения. Если нет возможности провести молекулярное тестирование, хирургическое удаление ЩЖ может быть рассмотрено для установления окончательного диагноза. |
| Bethesda V | 60-75% | Хирургическое лечение. Объем операции зависит от клинических факторов риска, сонографических особенностей, предпочтений пациента и, возможно, результатов мутационного тестирования (если оно проводилось).
Предпочтительный объем операции — тиреоидэктомия После рассмотрения клинических и сонографических особенностей мутационное тестирование на BRAF или панель маркеров мутации из семи генов ( BRAF , RAS , RET / PTC , PAX8 / PPARγ ) может быть рассмотрено в узлах с данным цитологическим заключением, если эти данные могут повлиять на принятие клинического решения и выбора объема операции. |
| Bethesda VI | 97-99% | Тиреоидэктомия |
Рекомендации по использованию системы Bethesda Корейской радиологической ассоциацией (Korean Society of Thyroid Radiology (KSThR) (2016)
| Результат ТАБ | Сонографические признаки узла K-TIRADS | Тактика |
| Bethesda-1 | Высокие подозрения
Средний или низкий уровень подозрений |
Повторная ТАБ в течение 3–6 месяцев
Повторная ТАБ в течение 6–12 месяцев |
| Bethesda-2 | Высокие подозрения
Средний или низкий уровень подозрений |
Повторная ТАБ в течение 6–12 месяцев
УЗИ через 12–24 месяца |
| Bethesda-3 | Высокие подозрения
Средний или низкий уровень подозрений. |
Повторная ТАБ в течение 3–6 месяцев
Повторная ТАБ в течение 6–12 месяцев. |
| Bethesda-4 | Все узлы | Диагностическая операция (гемитиреоидэктомия) |
| Bethesda-5 | Высокое или среднее подозрение
Низкое подозрение |
Хирургическое лечение
Повторная ТАБ или оперативное лечение. Активное наблюдение вместо немедленной операции может рассматриваться у взрослых пациентов с вероятной или доказанной папиллярной микрокарциномой |
| Bethesda-6 | Все узлы | Хирургическое лечение.
Активное наблюдение вместо немедленной операции может рассматриваться у взрослых пациентов с вероятной или доказанной папиллярной микрокарциномой |
Представленные рекомендации имеют некоторые отличия, но все они сводятся к тому, что при неинформативном или неопределенном результате необходимо повторить исследование. Если результат пункции не соответствует сонографической картине узла, то пункцию также следует повторить.
Необходимость и сроки повторной пункции должен определить ваш лечащий врач

УЗИ сканер HS50
Доступная эффективность. Универсальный ультразвуковой сканер, компактный дизайн и инновационные возможности.
Введение
Число пациентов с узловой патологией щитовидной железы (ЩЖ) в Республике Беларусь (РБ) и ряде регионов России неуклонно растет, что связывают с природным йодным дефицитом и последствиями катастрофы на Чернобыльской АЭС.
По данным Министерства здравоохранения РБ, распространенность узлового зоба в РБ составляет 102 на 100 000 человек.
Узловой зоб представляет собой весьма гетерогенную патологию щитовидной железы как с позиции морфологии, так и в плане клинического течения: речь может идти об узловом коллоидном зобе, узловой гиперплазии щитовидной железы, истинных или ложных кистах, аденоме щитовидной железы любого строения (фолликулярная, гюртлеклеточная, оксифильноклеточная), возможно сочетание узлового зоба и аутоиммунного тиреоидита или диффузного токсического зоба, кальцификатов в паренхиме щитовидной железы, а также злокачественных новообразований щитовидной железы [1-3]. Узловые образования щитовидной железы могут выявляться пальпаторно и/или при ультразвуковом исследовании (УЗИ). Широкое использование ультразвуковых аппаратов с высокой разрешающей способностью позволяет легко диагностировать узловые образования щитовидной железы, в том числе малых размеров (до 1 см в диаметре), у 19-67% лиц из случайной выборки [4-8]. Однако далеко не все изменения, выявляемые при УЗИ щитовидной железы, имеют клиническое и патологическое значение.
Главная цель диагностического поиска при узловом зобе — выявление пациентов с неопластическими изменениями щитовидной железы, так как именно эта категория больных в первую очередь подлежит хирургическому лечению и при необходимости радиойодотерапии, лучевой терапии и т.д.
Тонкоигольная аспирационная биопсия (ТАБ) щитовидной железы относится к методам прямой морфологической (цитологической) верификации различных заболеваний, проявляющихся узловым зобом, в том числе злокачественных новообразований щитовидной железы [9-12]. Тонкоигольная аспирационная биопсия пальпируемых узловых образований щитовидной железы может осуществляться под контролем как пальпации, так и УЗИ [13, 14]. Преимущества и недостатки технических вариантов проведения тонкоигольной аспирационной биопсии продолжают обсуждаться, однако доказано, что контроль с использованием УЗИ позволяет существенно повысить информативность тонкоигольной аспирационной биопсии, особенно когда речь идет об узловых образованиях с кистозным компонентом (10-25% всех узлов щитовидной железы), а также при решении вопроса о пункции наиболее подозрительного в отношении рака узловых образований при многоузловом зобе [15, 16].
Тонкоигольную аспирационную биопсию непальпируемых узловых образований щитовидной железы можно произвести только под контролем УЗИ. Существуют два основных варианта пункционной биопсии под контролем УЗИ — метод «свободной руки» и метод, связанный с применением пункционного адаптера, задающего пункционной игле фиксированное направление.
По данным многочисленных исследований, чувствительность тонкоигольной аспирационной биопсии в выявлении рака составляет 70-98% (в среднем около 80%), специфичность — 70-100% (в среднем 92%) [17-20].
По мнению большинства специалистов, показаниями к проведению тонкоигольной аспирационной биопсии при диагностике узлового зоба являются все пальпируемые узловые образования щитовидной железы, а также узловые образования размером 1 см и более [3, 20-22].
В то же время до сих пор в литературе имеют место противоречивые мнения о том, действительно ли существует необходимость выполнять тонкоигольную аспирационную биопсию всем пациентам с непальпируемыми (случайно выявленными) узловые образования размером до 1 см, не изучалась ранее также связь информативности тонкоигольной аспирационной биопсии под контролем УЗИ с размерами пунктируемых образований [4, 7, 8, 21].
Целью настоящей работы была оценка зависимости частоты выявления злокачественных и доброкачественных опухолей (неопластических изменений) щитовидной железы при тонкоигольной аспирационной биопсии щитовидной железы под контролем ультразвукового изображения от размеров пунктируемых узловых образований.
Материал и методы
В 2007 г. тонкоигольная аспирационная биопсия под контролем УЗИ была проведена амбулаторно 2281 пациенту (12% мужчин и 88% женщин в возрасте от 18 до 78 лет, в среднем 59 лет) по назначению врачей эндокринологов Витебска и Витебской области. Были пунктированы узловые образования различных структур и размеров. Под размером узловых образований понимали максимальный диаметр поперечного сечения узловых образований.
Пациенты, которым выполнялась тонкоигольная аспирационная биопсия под контролем УЗИ, были разделены на 3 группы:
- 1-я группа — 703 (30,8%) пациента, у которых диаметр поперечного сечения пунктированных узловых образований не превышал 0,9 см;
- 2-я группа — 802 (35,2%) пациента, у которых диаметр поперечного сечения пунктированных узловых образований составлял 1-1,5 см;
- 3-я группа — 776 (34,0%) пациентов, у которых диаметр поперечного сечения пунктированных узловых образований превышал 1,5 см.
УЗИ и контроль при проведении аспирационной пункционной биопсии осуществлялись на современном ультразвуковом аппарате с применением линейного датчика 7,5 МГц без биопсийного адаптера методом «свободной руки». Для каждого пункционного исследования использовался стандартный одноразовый инъекционный шприц объемом 10 мл с иглой 22G (0,7 мм).
Перед началом процедуры с каждым больным проводилась беседа об особенностях поведения при выполнении манипуляции. Пациент был информирован о том, что местное обезболивание не применяется, так как процедура является безболезненной, ее продолжительность составляет несколько минут, будут выполнены 1-2 аспирации, серьезные осложнения вследствие манипуляции возникают редко, но могут быть небольшая болезненность, припухлость и минимальная гематома в месте инъекции.
Пациентам сообщалось также об ограничениях этой диагностической процедуры — возможности получения неадекватного пунктата или так называемого «неопределенного» заключения цитологического исследования. После информированного согласия пациента на проведение инвазивного диагностического вмешательства манипуляция выполнялась без анестезии на операционном столе в присутствии медицинской сестры. Пациента укладывали на стол горизонтально, под плечи ему подкладывали валик, что способствовало расслаблению шейной мускулатуры. Врач, стоя справа от пациента, обрабатывал 70% раствором спирта кожу шеи в проекции узловых образований щитовидной железы. Узловые образования визуализировалось с помощью ультразвукового аппарата, после чего больному предлагалось несколько раз проглотить слюну, чтобы этого не произошло во время пункции. Затем подавалась императивная команда не разговаривать и не двигаться. После введения иглы в узел под контролем ультразвукового изображения выполнялись нескольких поступательных движений кончиком иглы внутри узла, далее датчик убирали с операционного поля и производили аспирацию ткани щитовидной железы. Слегка вытягивая поршень шприца, разрежение удерживали 5-10 с, пока содержимое узла не начинало поступать в канюлю иглы, затем разрежение снимали и иглу извлекали.
Обычно выполнялись 1-2 аспирации, в некоторых случаях их количество увеличивали до 4. Затем иглу отсоединяли от шприца, в него набирали 5 мл воздуха, иглу вновь присоединяли и по одной капле аспирированного материала наносили на каждое предметное стекло, после чего аспират аккуратно распределяли шлифовальным стеклом тонким слоем в одном направлении. Количество предметных стекол цитологического материала из каждого узла составляло в среднем 8-10 (от 1-2 до 12-14). Мазки высушивали естественным образом (на воздухе), после этого помещали в специальный контейнер для транспортировки в лабораторию.
Аспираты получали в основном из периферической части узла или из нескольких участков, чтобы повысить репрезентативность цитологического препарата. Пункции центральной части больших узлов старались избегать, так как там чаще всего находятся тканевой детрит и кистозное содержимое, образовавшиеся вследствие дегенерации узла, что снижает шанс получения информативного материала [9, 23-25].
Неоднородные узловые образования, особенно крупного размера, пунктировались в нескольких участках, имеющих различные плотность и структуру.
Основной проблемой тонкоигольной аспирационной биопсии кистозных узлов является получение неинформативных цитологических препаратов, не содержащих клеток [14], поэтому содержимое кист аспирировалось максимально полно, затем осуществлялась повторная тонкоигольная аспирационная биопсия солидного компонента узла. Аспирированная жидкость помещалась в пластиковый контейнер и направлялась на цитологическое исследование.
По окончании манипуляции накладывалась стерильная повязка, пациента просили посидеть несколько минут. Иногда больные жаловались на боль в месте биопсии или головокружение. Таких пациентов наблюдали в течение 1 ч, затем при отсутствии каких-либо изменений позволяли им уйти.
Препараты фиксировали эозин-метиленовым синим по Май — Грюнвальду и окрашивали рабочим раствором азур-эозина по Романовскому — Гимзе.
Поскольку главная цель диагностического поиска при узловой патологии щитовидной железы — выявление лиц, подлежащих хирургическому лечению, в группу анализируемых цитологических препаратов были включены информативные препараты, при исследовании которых было дано заключение о наличии у пациента неопластического процесса — «неоплазии», а также группа препаратов, подозрительных на злокачественные, по которым были даны предположительные заключения — «подозрение на неоплазию».
Ко второй группе анализируемых цитологических препаратов отнесли неинформативные препараты.
Цитологические препараты, по которым были диагностированы неопухолевые заболевания щитовидной железы (коллоидный пролиферирующий зоб, тиреоидиты, кисты), при проведении данного исследования не учитывались.
Информативными считались препараты, в которых определялись не менее 6 кластеров на каждом из двух стекол, с количеством клеток фолликулярного эпителия щитовидной железы не менее 10-15 [26], неинформативными — препараты, цитологический материал которых был представлен несколькими фолликулярными клетками или вообще без них, а также препараты, при фиксации и окрашивании которых были допущены технические погрешности.
В группу анализируемых цитологических препаратов с «подозрением на неоплазию» были отнесены следующие: с подозрением на фолликулярную неоплазию; на папиллярную карциному; на гюртлеклеточную неоплазию. В группу анализируемых цитологических препаратов «неоплазия» вошли: фолликулярная неоплазия, гюртлеклеточная неоплазия, папиллярная карцинома, медуллярная карцинома.
Цитологическая диагностика опухолей щитовидной железы проводилась в соответствии с Международной гистологической классификацией ВОЗ, исследование осуществлялось на основе общепринятых цитологических критериев дифференциальной диагностики основных форм рака щитовидной железы [27]. Формулировка цитологических заключений по тонкоигольной аспирационной биопсии осуществлялась в соответствии с рекомендациями Российской ассоциации эндокринологов по диагностике и лечению узлового зоба [20].
Основные цитологические признаки препаратов группы «неоплазия» представлены в табл. 1. В случае отсутствия всех указанных ниже цитологических критериев неопластического процесса, но при наличии двух-трех из них формулировалось заключение «подозрение на неоплазию». В связи с тем, что анапластическая карцинома, лимфома и метастазы экстратиреоидной опухоли при выполнении данного исследования нами не были выявлены, их цитологические признаки не приводятся.
Для оценки различий численных величин и значимости изменения неколичественных показателей в качестве метода непараметрической статистики использовался критерий согласия χ².
Результаты
В 1-й группе больных только в 4 из 703 случаев было получено цитологическое заключение «подозрение на неоплазию», заключение «неоплазия» не было сделано, в 169 случаях исследование оказалось неинформативным. Во 2-й группе в 24 из 802 случаев получено заключение «подозрение на неоплазию», у 8 пациентов поставлен диагноз «рак щитовидной железы» (у 6 — папиллярный, у 2 — медуллярный), в 56 случаях исследование оказалось неинформативным. Таким образом, признаки неопластической патологии в группе больных с размерами узловых образований 1-1,5 см выявлялись статистически значимо чаще, чем в группе больных с размерами узловых образований до 0,9 см (χ²=17,34; р<0,001). В 3-й группе в 26 из 776 случаев получено заключение «подозрение на неоплазию», у 10 пациентов поставлен диагноз «рак щитовидной железы» (у 9 — папиллярный, у 1 — медуллярный), в 51 случае исследование оказалось неинформативным. Таким образом, признаки неопластической патологии в группе больных с размерами узловых образований, превышающими 1,5 см, выявлялись статистически значимо чаще, чем в группе больных с размерами узловых образований до 0,9 см (χ²=21,70; р<0,001). При сравнении частоты выявления неопластических изменений при цитологическом исследовании во 2-й и 3-й группах (32 из 802 и 36 из 776) достоверных различий не удалось установить (χ²=0,26).
Таблица 1. Основные цитологические критерии дифференциальной диагностики основных форм рака щитовидной железы [27].
| Цитологические признаки | Папиллярная карцинома | Фолликулярная неоплазия | Медуллярная карцинома | Гюртлеклеточная неоплазия |
|---|---|---|---|---|
| Структуры | Сосочковые | Фолликулярные | Редко сосочковые и фолликулярные | Трехмерные солидные, трабекулярные, атипические микрофолликулы с нагромождением клеток |
| Клетки | Чаще без выраженного полиморфизма | Чаще без выраженного полиморфизма | Разнообразные типы: округлые, плазмоцитоидные, вытянутые и др. | Однородная популяция, полиморфные, много разрозненных клеток |
| Ядра | Округло-овальные | Округлые | Вариабельные, часто 2-3-4-ядерные | Крупные полиморфные, единичные многоядерные клетки |
| Мембрана ядер, борозды | Борозды часто | Относительно ровная, единичные борозды | Относительно ровная, единичные борозды | Неровная, с утолщениями, нередко борозды |
| Внутриядерные включения | Часто | Редко | Редко | Нередко |
| Хроматин | Стертый рисунок в виде «матового часового стекла» | Зернистый | Неравномерный глыбчатый (нередко в виде «соли-и-перца») | Неравномерный грубозернистый, нарастает число гиперхромных ядер |
| Ядрышки | Микроядрышки | Вариабельные | Микроядрышки | Полиморфные макроядрышки со смещением к периферии ядра |
| Цитоплазма | Плотная, полупрозрачная, с четкими контурами | Нежно структурированная, с нечеткими контурами | Розовая зернистость | Светлая, оксифильная, с четкими контурами |
| Дополнительные цитологические признаки | Псаммомные тельца | Коллоид | Амилоид | — |
Неинформативными оказались цитологические заключения у 24% пациентов из 1-й группы, у 7% — из 2-й группы и у 6,57% — из 3-й группы. Неинформативные заключения выявлялись статистически значимо чаще в 1-й группе, чем во 2-й (χ²=84,39; d<0,001) и в 3-й (χ²=87,51; р<0,001) группах. При сравнении частоты получения неинформативного заключения во 2-й и 3-й группах (56 из 802 и 51 из 776) также не удалось выявить достоверных различий (χ²=0,05).
Таблица 2. Результаты цитологического исследования пунктата щитовидной железы («подозрение на неоплазию» и «неоплазия») в 1-3.й группах пациентов.
| Группа обследованных | Размеры пунктированного узлового образования, см | Общее количество больных в группе | Количество больных с «подозрением на неоплазию» | Неоплазия | Неинформативные цитологические заключения | |||
|---|---|---|---|---|---|---|---|---|
| абс. | % | абс. | % | абс. | % | |||
| 1-я | ≤0,9 | 703 | 4 | 0,56 | 0 | 0 | 169 | 24 |
| 2-я | 1,0-1,5 | 802 | 24 | 2,99 | 8 | 0,99 | 56 | 7 |
| 3-я | ≥1,5 | 776 | 26 | 3,35 | 10 | 1,29 | 51 | 6,57 |
| Всего | от ≤ 0,9 до ≥1,5 | 2281 | 54 | 2,37 | 18 | 0,78 | 276 | 12,1 |
Таким образом, из 2281 пациента, которым проводилась пункция по поводу узловых образований щитовидной железы, признаки неопластической патологии были установлены у 3,15% (54, или 2,37% пациентов с цитологическим заключением «подозрение на неоплазию» и у 18, или 0,78% пациентов с цитологическим заключением «неоплазия»). В 12,1% случаев (276 пациентов) цитологические заключения оказались неинформативными (табл. 2).
При цитологическом исследовании кистозного содержимого узлов полученная при пункции жидкость центрифугировалась и осадок также переносился на предметные стекла. При микроскопии осадка, как правило, выяснялось, что он содержит лишь небольшое количество фолликулярных клеток, иногда с признаками пролиферации.
Обсуждение
При пальпации узловых образований щитовидной железы выявляются примерно у 4-5% людей, а при УЗИ — почти в 10 раз чаще [3, 4, 7, 11]. При этом наиболее часто узловой зоб встречается у женщин и лиц пожилого возраста [4, 5]. Зачастую непальпируемые узловые образования щитовидной железы обнаруживаются случайно, например, при УЗИ брахиоцефальных сосудов [4, 6, 28, 29]. При обнаружении в щитовидной железе пальпируемого солитарного узлового образования одной из главных целей обследования является исключение рака щитовидной железы. Вероятность наличия рака в пальпируемом солитарном узловом образовании составляет примерно 5% [11]. В регионах с йодным дефицитом многоузловой зоб имеет очень большую распространенность. Как и в случае солитарных узловых образований, здесь также необходимо исключать рак щитовидной железы. Долгое время считалось, что риск наличия рака в многоузловом зобе значительно ниже, чем в солитарных узлах, однако в дальнейшем было показано, что в том и другом случае он существенно не различается [11, 30]. По мнению К. Okour [28], тонкоигольная аспирационная биопсия пальпируемых узлов позволяет поставить правильный диагноз в 75% случаев, а при злокачественных узловых поражениях — более чем в 90% случаев. В связи с этим всем пациентам с пальпируемыми узловыми образованиями, за исключением функционально автономных, даже если речь идет о многоузловом зобе, необходимо выполнять тонкоигольную аспирационную биопсию. Что касается целесообразности проведения тонкоигольной аспирационной биопсии функционально автономных узловых образований, то этот вопрос должен решаться индивидуально, так как, по данным литературы, вероятность наличия рака в таких узловых образований крайне низка — 0,2-0,5% и проведение тонкоигольной аспирационной биопсии показано лишь в случаях, когда имеются веские клинические основания подозревать рак щитовидной железы (например, при быстром росте узла, его очень плотной консистенции и т. п.) [11].
Широкое использование в клинической практике ультразвуковых приборов с высокой разрешающей способностью позволило обнаружить значительную распространенность непальпируемых узловых образований щитовидной железы — так называемых инциденталом (от англ. «incidentalomas») [4]. Однако мнение о целесообразности проведения тонкоигольной аспирационной биопсии непальпируемых узловых образований весьма противоречивы, так как далеко не все изменения, которые выявляются при УЗИ щитовидной железы, имеют клиническое и патологическое значение.
По данным литературы, непальпируемые узловые образования при скрининговом УЗИ обнаруживаются у 20-50% всей популяции [29, 31, 32]. Непальпируемые узловые образования представляют собой гетерогенную группу: они могут быть множественными, солитарными и значительно варьировать по размеру. Недоступными пальпации могут оказаться и достаточно крупные узлы (>2 см) в силу того, что в случае сочетания с диффузным увеличением щитовидной железы они могут располагаться в глубине доли [7]. Использование ультразвукового контроля потенциально позволяет проводить тонкоигольную аспирационную биопсию узловых образований диаметром всего несколько миллиметров. Однако, по мнению ряда авторов [4, 8, 11], экономическая эффективность использования тонкоигольной аспирационной биопсии в качестве метода скрининга для диагностики неопластических изменений щитовидной железы представляется крайне низкой. Согласно данным литературы, только 3-4% мелких непальпируемых узловых образований могут быть злокачественными, причем большинство таких оккультных карцином не прогрессирует до клинически значимых стадий [11]. В ряде исследований показано, что, несмотря на относительно высокую распространенность оккультного рака щитовидной железы (около 36 случаев на 1000 населения, вариации от 4,5 до 356 случаев), клиническую значимость приобретает абсолютное меньшинство таких образований, поскольку распространенность клинически значимого рака щитовидной железы составляет лишь около 2,5 случая на 1000 населения [8]. Активный поиск и лечение оккультных карцином щитовидной железы, по мнению ряда авторов [4, 8, 11], сопряжен со значительными финансовыми затратами и необоснованной инвалидизацией пациентов.
Простота проведения УЗИ щитовидной железы, оснащенность ультразвуковыми аппаратами большинства лечебных учреждений и высокая распространенность тиреоидной патологии в популяции привели к тому, что УЗИ щитовидной железы сплошь и рядом стало выполняться «на всякий случай», т. е. многими лечебными учреждениями проводится негласное и не регламентированное ни одним эндокринологическим сообществом скрининговое УЗИ щитовидной железы. В ряде лечебных учреждений, в которых налажена тонкоигольная аспирационная биопсия, последняя зачастую проводится при любых, даже 2-4-миллиметровых образованиях. Если учесть стоимость УЗИ («скрининг»), самой пункции, а также работу лаборанта и специализирующегося на этих вопросах цитолога, то получится как раз та сумма, которая потрачена без особых оснований. Таким путем действительно можно обнаружить единичные случаи рака щитовидной железы, но, по мнению ряда исследователей, затраты на обследование огромного числа пациентов с целью поиска излечимого по современным представлениям заболевания не оправданы [33].
Представляют интерес экономические последствия так называемого непредвиденного (случайного) обнаружения узлов щитовидной железы при УЗИ, компьютерной и магнитно-резонансной томографии. После проведенных исследований в США установлено, что выявление (скрининг) заболеваний щитовидной железы (особенно ранних стадий рака щитовидной железы) с использованием указанных выше методов приводит к экономически необоснованному снижению качества жизни пациентов в результате последующего лечения, причем основное внимание уделяется тому факту, что с использованием высокотехнологичных методов диагностики смертность от рака щитовидной железы не снижается, а затраты на каждого пациента повышаются в среднем на 1200 долларов США [34].
Согласно клиническим рекомендациям Российской ассоциации эндокринологов по диагностике и лечению узлового зоба [20], показаниями к проведению тонкоигольной аспирационной биопсии в рамках диагностики узлового зоба являются следующие.
- Узловые образования щитовидной железы, равные или превышающие в диаметре 1 см (выявленные при пальпации и/или УЗИ).
- Проведение тонкоигольной аспирационной биопсии при случайно выявленных образованиях меньшего размера целесообразно только при подозрении на злокачественную опухоль щитовидной железы по данным УЗИ при условии технической возможности выполнить пункцию под контролем УЗИ.
- Клинически значимое увеличение ранее выявленного узлового образования щитовидной железы при динамическом наблюдении. Тонкоигольная аспирационная биопсия сама по себе не является методом динамического наблюдения при узловом зобе и при отсутствии прогрессирующего
- роста последнего периодическое проведение тонкоигольной аспирационной биопсии не показано.
Специалистами Американского общества ультразвуковой диагностики в 2005 г. были сформулированы положения Консенсуса, регламентирующего тактику ведения пациентов с узловой патологией щитовидной железы с размерами узловых образований 1 см и более (табл. 3) [21]. Эти рекомендации применимы только для узловых образований, размеры которых превышают 1 см, так как, с точки зрения американских специалистов, весьма спорным является утверждение, что диагноз микрокарциномы размерами менее 1 см или даже рака размерами менее 2 см с последующим хирургическим лечением улучшит качество и продолжительность жизни пациента. Кроме того, по мнению американских экспертов, включение узловых образований размерами до 0,9 мм в категорию необходимых для тонкоигольной аспирационной биопсии привело бы к неоправданному увеличению числа биопсий [22].
С точки зрения специалистов Американской ассоциации клинических эндокринологов (AACE), тонкоигольная аспирационная биопсия узловых образований размерами 10 мм и менее не показана, если результаты УЗИ не подозрительны в отношении рака щитовидной железы и отсутствует высокий риск рака по данным анамнеза. При всех гипоэхогенных узловых образований размером более 10 мм, имеющих неровные контуры, неправильную форму, кальцинаты, хаотичный интранодулярный кровоток, требуется выполнение тонкоигольной аспирационной биопсии под контролем УЗИ. Если при УЗИ получены данные, позволяющие заподозрить экстракапсулярный рост или метастатический процесс в шейных лимфатических узлах, цитологическое исследование показано независимо от размеров узловых образований. Пациентам, которым, по данным анамнеза, проводили облучение головы и шеи, а также при отягощенном анамнезе по раку щитовидной железы тонкоигольная аспирационная биопсия под контролем УЗИ также показана, даже если размер узловых образований не превышает 10 мм [3, 21, 22].
Пациентов со случайно выявленными узловыми образованиями щитовидной железы (инциденталомы) целесообразно обследовать при помощи УЗИ через 6-12 мес и периодически в дальнейшем [22].
Согласно рекомендациям специалистов Американской тиреоидологической ассоциации (АТА), специальное обследование требуется только при выявлении узловых образований диаметром более 1 см, поскольку именно они могут оказаться клинически значимым раком [3].
Однако все эти рекомендации не являются абсолютными и в определенных ситуациях оставляют за врачомклиницистом право на решение вопроса о необходимости тонкоигольной аспирационной биопсии даже в тех случаях, когда узловые образования не отвечают указанным выше критериям.
Таблица 3. Рекомендации Американского общества специалистов ультразвуковой диагностики по ведению узловой патологии щитовидной железы при размере узловых образований 1 см и более [21].
| Ультразвуковой признак | Рекомендации тонкоигольной аспирационной биопсии | |
|---|---|---|
| Солитарный узел: | ||
| с микрокальцинатами | Строго рекомендована тонкоигольная аспирационная биопсия при размерах узла ≥ 1 см | |
| с кальцинатами больших размеров | Строго рекомендована тонкоигольная аспирационная биопсия при размерах узла ≥ 1,5 см | |
| солидно-кистозной структуры или кистозной структуры с пристеночным тканевым компонентом | Рекомендована тонкоигольная аспирационная биопсия при размерах узла ≥ 2 см | |
| имеет место рост узла по сравнению с результатами предыдущих УЗИ | Рекомендована тонкоигольная аспирационная биопсия | |
| полностью кистозная структура узла при отсутствии всего перечисленного выше | Не рекомендована тонкоигольная аспирационная биопсия | |
| Многоузловой зоб | Биопсия одного или нескольких узлов с приоритетом по указанным выше критериям (как и при солитарных узлах) |
Выводы
- В группе, состоявшей из 2281 пациента, у которого была выполнена тонкоигольная аспирационная биопсия щитовидной железы под контролем ультразвукового изображения, узловые образования размерами до 0,9 см определялись в 31% случаев, 1-1,5 см — в 35%, 1,5 см и более — в 34% случаев.
- Неинформативные цитологические заключения встречались статистически значимо чаще в группе пациентов с размерами узловых образований до 0,9 см (24%) по сравнению с группами пациентов с размерами узловых образований 1-1,5 см (7%), 1,5 см и более (6,6%). Статистически значимых различий в частоте получения неинформативных заключений в группах больных с размерами узловых образований 1-1,5 и 1,5 см и более не выявлено.
- При цитологическом исследовании частота выявления неопластических изменений в группах больных с размерами узловых образований 1-1,5 и 1,5 см и более была примерно в 4 раза выше, чем в группе пациентов с размерами узловых образований до 0,9 см. Статистически значимых различий в частоте неопластических изменений в группах больных с размерами узловых образований 1-1,5 и 1,5 см и более не выявлено.
Литература
- Данилова Л.И. Болезни щитовидной железы и ассоциированные с ними заболевания. Минск-Nagasaki: Heuwadou offset 2005; 470 с.
- Hegedus L. Clinical practice. The thyroid nodule // J. N. Engl Med 2004; 351: 1764-1771.
- Cooper D.S., Doherty G.M., Haugen B.R. et al. Management Guidelines for Patients with Thyroid Nodules and Differentiated Thyroid Cancer. The American Thyroid Association Guidelines Taskforce. Thyroid 2006; 16(2): 1-33.
- Тan G.H., Gharib H. Thyroid incidentalomas: management approaches to nonpalpable nodules discovered incidentally on thyroid imaging // J. Ann. Intern. Med. 1997; 126: 226-231.
- Wienke J.R., Chong W.K., Fileding J.R. et al.// J. Ultrasound. Med. 2003; 22: 1027-1031.
- Brander A., Viikinkoski P., Tuuhea J. et al. Clinical versus ultrasound examination of the thyroid gland in common clinical practice // J. Clin. Ultrasound. 1992; 20: 37-42.
- Brander A., Viikinkoski P., Nickels J., Kivisaari L. Thyroid gland: US screening in a randomize adult population // Radiology 1991; 181: 683-688.
- Wang C., Crapo L.M. The epidemiology of thyroid disease and implication for screening // J. Endocrinol. Metab. Clin. North. Am. 1997; 26: 189-218.
- Braga M., Cavalcanti T.C., Collaco L.M., Graf H. Efficacy of ultrasound-guided fine-needle aspiration biopsy in the diagnosis of complex thyroid nodules // J. Clin. Endocrinol. Metab. 2001; 86: 4089-4091.
- Marqusee E., Benson C.B., Frates M.C. et al. // J. Ann. Intern. Med. 2000; 1339: 696-700.
- Belfiore A., La Rosa G.L. Fine-needle aspiration biopsy of the thyroid // J. Endocrinol. Met. Clin. North. Am. 2001; 30: 361-400.
- Атабекова Л.А., Васильченко С.А., Бурков С.Г. Комплексная ультразвуковая и цитологическая оценка пролиферативных процессов в щитовидной железе // SonoAce-International 1999; 4: 60-65.
- Alexander E.K., Heering J.P., Benson C.B. et al. // J. Clin. Endocrinol. Metab. 2002; 87: 4924-4927.
- Gharib H., Goellner J.R., Johnson D.A. Fine-needle aspiration cytology of the thyroid. A 12-year experience with 11,000 biopsies // J. Clin. Lab. Med. 1993; 13: 699-709.
- Carmeci С., Jeffrey R.В., McDougall I.R. et. al. Ultrasound-Guided Fine-Needle Aspiration Biopsy of Thyroid Masses // Thyroid. 1998; 8(4): 283-289.
- Takashima S., Fukuda H., Kobayashi T. Thyroid nodules: clinical effect of ultrasound-guided fineneedle aspiration biopsy // J. Clin. Ultrasound. 1994; 22(9): 535-542.
- Ольшанский В.О., Сергеев С.А., Трофимова Е.Ю. и др. Клиническая оценка ультразвукового метода и выбор оптимального объема оперативного вмешательства у больных с опухолями щитовидной железы. Методические рекомендации. М., 1997; 7 с.
- Katagiri M., Harada Т., Kiyono T. Diagnosis of thyroid carcinoma by ultrasonic examination: comparison with diagnosis by fine-needle aspiration cytology // J. Thyroidol. Clin. Exp. 1994; 6(1): 21-26.
- Yokozawa Т., Miyauchi A., Kuma К., Sugawara M. Accurate and Simple Method of Diagnosing Thyroid Nodules by Modified Technique of Ultrasound-guided fine-needle Aspiration Biopsy // Thyroid 1995; 5(2): 141-145.
- Клинические рекомендации Российской ассоциации эндокринологов по диагностике и лечению узлового зоба // Проблемы эндокринологии 2005; 5: 40-42.
- Frates M.C., Benson C.B., Charboneau J.W. et al. Management of thyroid nodules detected at US: Society of Radiologists in Ultrasound Consensus Conference Statement // J. Radiology. 2005; 237: 794-800.
- American Association of clinical Endocrinologists medical guidelines for the Diagnosis and Management of Thyroid Nodules. AACE/AME. Task Force on Thyroid Nodules // J. Endocr. Pract. 2006; 12: 63-102.
- Musgrave Y.M., Davey D.D., Weeks J.A. Assessment of fine-needle aspiration sampling technique in thyroid nodules // J. Diagn. Cytopathol. 1998; 18: 76-80.
- La Rosa G.L., Belfiore A., Giuffrida D. et al. Evaluation of the fine needle aspiration biopsy (FNAB) in the preoperative selection of «cold» thyroid nodules // J. Cancer. 1991; 67: 2137-2141.
- Ravetto C., Colombo L., Dottorini M.E. Usefulness of fine-needle aspiration in the diagnosis of thyroid carcinoma: a retrospective study in 37 895 patients // J. Cancer. 2000; 90: 357-363.
- Hamburger J.I. Diagnosis of thyroid nodules by fine needle biopsy: Use and abuse // J. Clin. Endocrinol. Metab. 1994; 79: 335-339.
- Шапиро Н.А., Камнева Т.Н. Цитологическая диагностика заболеваний щитовидной железы. Цветной атлас. Пособие для врачей. М., 2003; 172 с.
- Okour K.I. Заболевания щитовидной железы — сравнение ультразвукового и других методов исследования // SonoAce-International. 1999, 5: 51-59.
- Зайратьянц О.В. Эпидемиология и этиологическая структура узлового зоба по данным аутопсий. ТИРОНЕТ 2002; 5: 6 thyronet.rusmedserv.com
- McCall A., Jarosz H., Lawrence A.M., Paloyan E. The incidence of thyroid carcinoma in solitary cold nodules and in multinodular goiter // Surgery. 1986; 100: 128-132.
- Bruneton J.N., Balu-Maestro C., Marcy P.Y. et al. Very high frequency (13 MHz) ultrasonographic examination of the normal neck: Detection of normal lymphnodes and thyroid nodules // J. Ultrasound. Med. 1994; 13: 87-90.
- Mortensen J.D., Woolner L.B., Bennett W.A. Gross and microscopic findings in clinically normal thyroid glands // J. Clin. Endocrinol. 1955; 15: 1270-80.
- Фадеев В.В. Узловые образования щитовидной железы: международные алгоритмы и отечественная клиническая практика // Врач 2002; 7: 12-16.
- Ванушко В.Э., Кузнецов Н.С. Медицинские и экономические аспекты хирургии узлового зоба. Эндокринологический научный центр РАМН.

УЗИ сканер HS50
Доступная эффективность. Универсальный ультразвуковой сканер, компактный дизайн и инновационные возможности.
Биопсия щитовидной железы
Об органе
Щитовидная железа – орган маленький (около 4 см в высоту и весом 20 граммов), по форме бабочку, расправившую крылья напоминающий. Однако именно на нем лежит огромная ответственность за обмен веществ в нашем организме, сердечно-сосудистую и нервную системы, половую активность и психоэмоциональную сферу.
Находится орган в передней части шеи, пониже адамова яблока. Железа охватывает трахею и, будучи органом очень мягким, в нормальном состоянии не обнаруживается. Прощупывается и бывает хорошо видна, она в стадии какой-либо патологии.
Медицинская статистика говорит нам: у женщин проблемы, связанные с щитовидной железой, возникают чаще, нежели у мужчин. Отчасти это объясняется тем, что представительницы прекрасного пола вынуждены больший период своей жизни проводить в циклическом режиме, определяющемся попеременной активностью 2-х половых гормонов-антагонистов – прогестерона и эстрогена.
Функции
Как уже было отмечено, несмотря на свои крохотные размеры, щитовидная железа выполняет крайне важные функции в нашем организме, влияет на:
- Рост органов;
- Нервную систему;
- Процессы психического характера;
- Минеральный баланс;
- Углеводное, белковое и жировое равновесие;
- Репродуктивную функцию и другое.
Немаловажно, что щитовидная железа вырабатывает тиреоидные гормоны, используя содержащийся в пище йод.
О процедуре
Биопсия является наиболее информативным и точным методом современной диагностики. Что касается раковых заболеваний щитовидной железы, он наиболее удобен, так как с его помощью можно определить характеристики узловых образований менее чем 1 см.
Конечно же, традиционным показанием к проведению процедуры является обнаружение у больного опухоли размером 1 и более сантиметров. При этом, если после УЗИ есть подозрение на рак, биопсия может быть проведена, даже если опухоль менее 1 см. К этой же категории относятся люди, чьи родственники болели онкологией щитовидной железы любо подвергались облучению.
Таким образом, когда возникает подозрение на опухолевый процесс в органе, а также в целях скрининга выбирают тонкоигольную аспирационную пункционную биопсию.
Это единственный вариант выявить опухоль до момента хирургической операции. Именно поэтому сегодня мы видим значительное снижение числа операционных манипуляций на органе.
Методика проведения
Первый этап биопсии – это забор биоптата. Сама процедура быстрая, малотравматичная, почти безболезненная, поэтому не требует специальной подготовки, и проводят ее в условиях амбулатории. Иногда используют местную анестезию. Длительность процедуры – до двух минут.
Для проведения процедуры используют контроль УЗИ. Это позволяет точно определить место прокола. Кожу прокалывают тонкой иглой и вводят ее в ткань опухоли.
Взяв с помощью иглы биоптат (материал для дальнейшего лабораторного изучения), иглу извлекают. Обычно врач делает 1-3 пункции: необходим материал из нескольких мест.
Вторая часть – это лабораторное цитологическое исследование забранного материала.
Результаты
Результаты исследования могут подтвердить или же опровергнуть предварительный диагноз.
Все выводы исследования основаны на рекомендациях мирового содружества цитологов.
Заключения могут быть следующими:
- Узел доброкачественный («коллоидный»). Он не требует лечения и в рак не перерождается.
- Опухоль раковая.
- Аутоиммунный тиреоидит (Тиреоидит Хашимото). Это воспаление ткани щитовидной железы, вызванного агрессией собственной иммунной системы.
- Опухоль фолликулярная. Имеет злокачественную сущность примерно 20%. Чтобы такой диагноз уточнить, узел полностью удаляют, исследуя его капсулу. Только после этого можно установить, был ли узел фолликулярным раком или же являлся аденомой.
- Заключение неинформативное. Возникает из-за того, что в биоптате разные клетки. Чтобы установить диагноз, необходимо через определенное время процедуру
Клиника интегративной онкологии Onco.Rehab – всегда на страже Вашего здоровья. Обратитесь и получите направление на проведение биопсии у наших надежных партнеров.
- A
- Б
- В
- Г
- Д
- Е
- Ж
- З
- И
- К
- Л
- М
- Н
- О
- П
- Р
- С
- Т
- У
- Ф
- Х
- Ц
- Ч
- Ш
- Щ
- Э
- Ю
- Я
Статья на конкурс «био/мол/текст»: Рак — та проблема, которая так или иначе волнует каждого из нас, а некоторых, к сожалению, коснулась напрямую. Сегодня заболеваемость онкологическими патологиями неуклонно растет. Однако сейчас мы бы хотели поговорить с вами о том виде рака, который бояться в большинстве случаев совсем не нужно! Это рак щитовидной железы. Заинтригованы? Читайте эту статью.
Несомненно, XXI век — время развития научно-технического прогресса. Вместе с совершенствованием технологий приходит и их доступность в повсеместном использовании. Медицина не является исключением. Благодаря развитию технологий диагностики и лечения самых разных заболеваний мы стали спасать тех пациентов, которые когда-то входили в число неизлечимых. Однако не на все сферы медицины прогресс повлиял так положительно. Поэтому сегодня мы бы хотели познакомить вас с такими животрепещущими вопросами медицины, как гипердиагностика и гиперлечение. Сейчас мы остановимся лишь на одной, но весьма значимой стороне данной проблемы — гипердиагностика узлов щитовидной железы, а также гиперлечение этих узлов и рака щитовидной железы.
Что мы знаем сегодня про узлы щитовидной железы?
26 сентября 2019 года в группе «Медфронт» во «ВКонтакте» появилась небольшая статья Александра Циберкина, врача-эндокринолога, создателя блога «Занимательная эндокринология» [1]. Проблема, которая поднималась в статье, достаточно проста: многим из нас когда-то предлагали сделать УЗИ щитовидной железы на всякий случай. На наш взгляд, Александр рассказывает о проблеме гипердиагностики и гиперлечения для того, чтобы врачи всерьез задумались, правильно ли назначать не всегда нужные анализы всем, и насколько серьезной проблемой является обнаружение узла в щитовидной железе в процессе такого скрининга.
Однако то, что эта проблема была озвучена совсем недавно, не значит, что о ней больше не надо писать. Мы не хотим загружать вас медицинской терминологией, вновь писать о TI-RADS и разбирать по кусочкам, что может написать функциональный диагност в заключении. Мы обращаемся к вам в качестве потенциальных пациентов и хотим донести мысль, что не всегда узел в щитовидной железе опасен, а рак априори смертелен.
База, с которой нам нужно познакомиться: щитовидная железа
Немножко о щитовидной железе (ЩЖ). Это орган эндокринной системы человека, который располагается на передней поверхности шеи в области гортани, прямо перед щитовидным хрящом. Состоит железа из левой и правой долей и перешейка. ЩЖ богато кровоснабжается разными артериями, а иннервируется гортанными нервами.
Главной функцией щитовидной железы (лат. glandula thyroidea) является синтез тиреоидных гормонов, необходимых нашему организму. Под тиреоидными гормонами мы подразумеваем два соединения: тироксин (Т4) и трийодтиронин (Т3). Основной функцией Т4 и Т3 является увеличение потребления клетками кислорода. Иначе говоря, эти гормоны стимулируют все энергетические процессы в клетке и обмен веществ, причем их влияние распространяется на все клетки организма.
Также клетки ЩЖ производят кальцитонин, ответственный за обмен кальция в организме.
Прямо за щитовидной железой располагаются четыре небольшие паращитовидные железы. Последние производят паратиреоидный гормон, который также отвечает за поддержание уровня кальция в организме, причем в большей степени, чем кальцитонин.
Откуда берется столько случаев рака щитовидки?
Рак щитовидной железы (РЩЖ) — наиболее распространенное злокачественное новообразование эндокринной системы [2]. Все чаще мы слышим, что заболеваемость РЩЖ неуклонно растет. И звучит это ужасающе, однако так ли всё просто на самом деле? Возможно, вы будете шокированы, какая правда скрывается за этими, на первый взгляд, однозначными научными фактами. И прежде, чем мы разберемся с истинной причиной роста заболеваемости РЩЖ, необходимо ознакомиться с тем, какие виды рака щитовидки существуют.
Итак, начнем. Сейчас нам понадобится привести немного численных данных, но не пугайтесь их, всё крайне просто. В научном сообществе выделяют пять типов РЩЖ:
- Папиллярный (80–85% случаев).
- Фолликулярный (10–15% случаев).
- Медуллярный (5% случаев).
- Низкодифференцированный (1% случаев).
- Недифференцированный (0,1–0,2% случаев).
Наиболее благоприятными принято считать два первых типа РЩЖ. И как мы можем заметить, они встречаются наиболее часто. Их также называют высокодифференцированными типами рака. Медуллярный, низкодифференцированный и недифференцированный типы считаются агрессивными формами РЩЖ. В нашей статье мы сделаем акцент лишь на первых двух типах РЩЖ, так как они являются наиболее распространенными.
Что означает понятие «дифференцировка»?
Когда-то давно, еще до нашего рождения, каждый из нас представлял собой одну-единственную клетку. Во время внутриутробного развития клеток стало в триллионы раз больше! И каждая из них обрела свою собственную функцию: одни отвечают за биение нашего сердца, другие защищают наш организм от внешних и внутренних опасностей, а третьи отвечают за когнитивные функции. И таких видов клеток более 230! Путь, который проходит клетка от той единственной, стоявшей в начале нашего пути, до высоко специализированной клетки, у которой есть четкие обязанности, и называется «дифференцировка».
Что касается рака — если клетки, из которых состоит опухоль, являются высокодифференцированными, в большинстве случаев врачи считают исход благоприятным. Однако если опухоль состоит из низкодифференцированных клеток, то с большой вероятностью она склонна к агрессивному течению. Как уже было сказано, наиболее часто выявляемые РЩЖ являются высокодифференцированными.
Папиллярный РЩЖ — наиболее распространенная форма: 80–85%. И с самым хорошим прогнозом. Пятилетняя выживаемость пациентов с РЩЖ — 98,1% [2]. Что это значит для пациента? Что наиболее часто выявляемые случаи РЩЖ имеют благоприятный исход!
Рак, ушедший в себя
Наше традиционное понимание РЩЖ, а именно его развития, в корне изменилось благодаря трем исследованиям 2014 года (Thyroid cancer trilogy) [3–5]. Казалось бы, все злокачественные образования по мере развития подвергаются прогрессии, а потому нуждаются в ранней диагностике и оперативном лечении. Впервые за всю историю человека было обнаружено существование «самоограничивающихся раков» (self-limiting cancers), которые являются злокачественными, но при этом не прогрессируют в летальные формы из-за ограниченной способности к делению клеток, составляющих опухоль. Конечно же, существуют и так называемые летальные РЩЖ (lethal thyroid cancers). Различие между ними заключается в происхождении раковых клеток, что и определяет развитие заболевания и его исход. Во втором случае клетки как бы затаиваются на долгий срок, на годы и даже на десятилетия, а потом по невыясненным еще причинам внезапно начинают делиться и приводят к неблагоприятному исходу. Однако на данный момент считается, что именно «самоограничивающиеся» типы РЩЖ составляют большинство.
Подбираемся к корню проблемы: статистика и диагностика
Вернемся к распространенности РЩЖ. Теперь мы готовы понять, что возросшее число случаев данной патологии не является поводом для беспокойства.
В 1975 году заболеваемость РЩЖ составляла 4,9 на 100 000 человек и оставалась относительно стабильной до начала 1990-х годов [6]. За последние 25 лет заболеваемость РЩЖ выросла более чем в 3 раза, то есть на 300% (рис. 1) [7], [8], причем в большинстве случаев за счет высокодифференцированного папиллярного РЩЖ. При этом очень важно понимать, что, несмотря на такой значительный рост, смертность от РЩЖ остается стабильной, примерно 0,5 случаев на 100 000 человек [6].
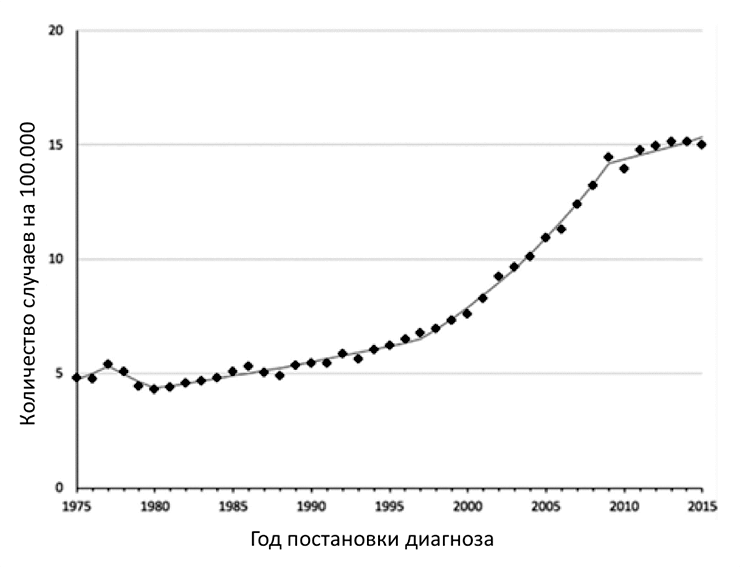
Рисунок 1. Данные заболеваемости раком щитовидной железы в период с 1975 по 2015 годы
Чувствуете, что тут что-то не так? Нет связи между возросшим числом случаев РЩЖ и смертностью от этой патологии! Среди врачей и ученых до сих пор продолжаются дебаты, почему так происходит. Сейчас выделяют несколько теорий. Наиболее вероятная — широкое распространение методов ультразвуковой диагностики (УЗИ). Пусть корни УЗИ уходят к Леонардо да Винчи и XV веку, широкое медицинское распространение данный метод получил с 50-х годов XX века [9], [10]. Сегодня УЗИ является наиболее простым, дешевым, неинвазивным и информативным методом выявления опухолевых образований щитовидной железы. Поэтому, как вы можете догадаться, УЗИ стали делать почти всем, причем независимо от показаний.
Сейчас научное сообщество активно дискутирует на тему, связаны ли такие показатели с истинным увеличением заболеваемости РЩЖ, или же проблема в гипердиагностике тех небольших образований ЩЖ, которые не требуют никакого вмешательства со стороны человека [11], [12].
Для более полного понимания проблемы вернемся на чуть более ранний этап диагностики РЩЖ.
Что такое узлы и как их найти?
Узлы ЩЖ — это радиологически различимые объемные образования в ЩЖ, которые могут быть доброкачественными и злокачественными. Узлы можно найти в 50% случаев всех проводимых УЗИ ЩЖ. При этом только 5% выявляемых образований будут злокачественными [13], [14].
Весомый вклад УЗИ в возросшее количество диагностированных узлов и РЩЖ можно показать на примере одного нашумевшего исследования в Южной Корее [3], [15], [16]. В 1999 году там была утверждена национальная программа, направленная на скрининг злокачественных заболеваний. Под программу попала и щитовидная железы. В результате повсеместного внедрения УЗИ щитовидки частота выявления рака выросла в 15 (!) раз с 1993 по 2011 год. И это мы еще не говорим просто об узлах, которые также могут быть психологической проблемой пациента. Большинство выявляемых случаев — папиллярный РЩЖ. Как вы помните, этот вид рака имеет весьма благоприятный исход. Однако простому населению идея жить с раком настолько чужда и неприятна, что было проведено огромное число полного удаления щитовидных желез, причем часто без видимой на то необходимости! А такая операция имеет серьезные последствия, о которых мы расскажем чуть ниже.
Врачи, осознав свою ошибку, убрали УЗИ щитовидки из списка обязательных скрининговых тестов. И результат не заставил себя ждать. В последней на эту тему публикации 2015 года сказано, что на 30% снизилась заболеваемость РЩЖ, а число операций на щитовидной железе снижалось на 35% ежегодно. Вывод напрашивается сам собой: в основе увеличения числа диагностированных случаев узлов щитовидки (в том числе и РЩЖ) является ставшее таким доступным УЗИ.
Думаем, следует также сказать, что образования ЩЖ выявляются не только при выполнении УЗИ, но и при использовании других методов лучевой диагностики (КТ, МРТ, ПЭТ), что стало возможным благодаря улучшению разрешающей способности оборудования. Следовательно, увеличилось чисто случайно выявляемых образований щитовидной железы (в том числе, рака) — инциденталóм (от англ. incidence — случайность) [17]. Инциденталомы клинически никак себя не проявляют и могут оставаться в организме бессимптомно всю жизнь. И многие из таких инциденталом обнаруживались лишь посмертно, случайно, и не являлись причиной кончины человека. Это позволяет говорить нам о существовании резервуара пациентов с узлами или раком щитовидной железы, который клинически является скрытым и никак себя не проявляет до его случайного обнаружения [18].
Приведенные данные обобщены на рисунке 2.

Рисунок 2. Что даст нам УЗИ щитовидки на самом деле?
рисунок авторов статьи
Напомним, что в нашей статье мы делаем акцент на наиболее распространенных типах РЩЖ (папиллярный, фолликулярный). Агрессивные формы РЩЖ (медуллярный, низкодифференцированный, недифференцированный и редко папиллярный) требуют дальнейшего более детального изучения
Самое главное: почему гипердиагностика и гиперлечение РЩЖ являются проблемой?
Является ли столь чрезмерное выявление объемных образований ЩЖ проблемой? Да, и очень даже серьезной. И она получила свое название — гипердиагностика (overdiagnosis) [19], [20]. И проблема состоит в том, что следствием ее становится гиперлечение. На самом деле она касается не только ЩЖ и представляет более серьезную опасность, чем может казаться на первый взгляд, а по мере развития методов диагностики приобретает все более и более масштабный характер, о чем говорит в своей статье «На всякий случай…» врач-эндокринолог В.В. Фадеев [28]. Говоря о ЩЖ, большинство пациентов с папиллярным РЩЖ подвергаются оперативному лечению — тотальной тиреоидэктомии или гемитиреоидэктомии [21]. Тем не менее в некоторых исследованиях [22], [23] показано, что при выборе лечения в пользу «активного наблюдения» (active surveillance) у пациентов с папиллярным РЩЖ (который относится к low-risk РЩЖ) диаметром менее одного сантиметра обнаруживались такие же исходы заболевания, как и при выполнении хирургических операций. В связи с этим в 2015 году в клинических рекомендациях Американской тиреоидологической ассоциации (American thyroid association, ATA) впервые была принята стратегия «активного наблюдения» для пациентов с low-risk cancers [24].
В связи с выявленным фактом, что в оперативном лечении таких РЩЖ, вполне возможно, нет необходимости (а ведь удаление ЩЖ сопровождается серьезными последствиями, о чем мы расскажем далее), с 2015 года в США уже принимаются меры по снижению частоты гипердиагностики и гиперлечения [24]. Например, уже настоятельно рекомендовано не проходить скрининг РЩЖ пациентам, у которых нет никаких симптомов, поскольку выявление агрессивных типов рака в этом случае крайне маловероятно.
Еще одной мерой предотвращения гиперлечения является изменение классификации типов РЩЖ, которые ведут себя как доброкачественные. Иначе говоря, их больше не называют «рак». Зачем? Все дело в психологической реакции пациента. Инстинкт самосохранения — самый живучий инстинкт человека и животных. И реализуется он во многом благодаря страху. Благодаря страху антилопа убегает ото льва, а змея жалит потенциальный объект угрозы — животные стремятся выжить. То же и с человеком. Всеми способами человек хочет продлить свое существование на этой земле. И диагноз «рак», который социум привык ассоциировать c мучительным завершением жизни, заставляет человека сделать все, чтобы от этого самого рака избавиться. В нашем случае, если у человека нашли РЩЖ, самая стойкая мысль — избавиться от этого мучения. И в большинстве случаев выбор падает на полное удаление щитовидной железы, вне зависимости от того, необходимо ли это. Как говорится, на всякий случай. И во многих случаях это не оправдано.
В одном из исследований [25] было выяснено, что люди, как правило, имеют общее представление о РЩЖ, но не знают о его диагностике и лечении, полагая, что по распространенности и смертности РЩЖ схож с другими типами рака. Страх дальнейшего прогрессирования заболевания заставляет пациента выбирать радикальное лечение. Так, недавно проведенные исследования неинвазивного рака груди [24], [25], а впоследствии и папиллярного РЩЖ [25], показали влияние терминологии на выбор лечения: замена термина «рак» в описании обоих патологических состояний способствовала выбору пациентом нехирургического лечения. Таким образом, данная стратегия оказывает влияние на психологическое состояние пациентов, тем самым предотвращая гиперлечение. Возможно ли жить с диагнозом «рак»? Как бы ответили на этот вопрос вы?
Что врачи думают о данной проблеме?
Проблема гиперлечения РЩЖ существует не только среди пациентов, но и среди медицинского сообщества.
Конечно, выбор, удалять ли щитовидную железу или нет, стоит больше перед пациентом, нежели перед лечащим врачом. И пациент вполне может выбрать хирургическую тактику лечения. А врач должен определять, сколько ткани щитовидной железы в конкретном случае нужно убирать.
В качестве уменьшения гипердиагностики Американская тиреоидологическая ассоциация рекомендует воздержаться от скрининга и биопсии мелких образований щитовидной железы при отсутствии на то иных клинических симптомов [6].
Как вообще лечат рак щитовидной железы?
Давайте разберемся, какие существуют пути лечения РЩЖ [26].
- Полное удаление ЩЖ, тотальная тиреоидэктомия, вместе с окружающей клетчаткой, а иногда и рядом лежащими лимфатическими узлами.
- Терапия радиоактивным йодом I131 после тотальной тиреиодэктомии. Не пугайтесь — это не опасно! Такой йод влияет только на клетки щитовидной железы и убивает их.
Почему мы, авторы, так не хотим, чтобы щитовидную железу удаляли без серьезных на то причин? Казалось бы, мы уберем орган, где сидит рак, и будем жить себе спокойно, только лишь принимая препараты гормонов щитовидной железы. Это ведь лучше, чем жить с раком. Или все-таки нет? Так вот, сама сложность вопроса заключается в операции.
Чем чревато полное удаление щитовидки (или, как говорят врачи, тотальная тиреоидэктомия)?
Существует два серьезных осложнения тотальной тиреоидэктомии [27].
- Стойкое снижение функции щитовидной железы (гипопаратиреоз). Наиболее серьезное и жизнеугрожающее осложнение. Итак, прямо за щитовидной железой располагаются четыре паращитовидные железы. Они производят паратиреоидный гормон, который отвечает за обмен кальция в нашем организме (а из него состоит бóльшая часть наших костей!). Паращитовидные железы совсем маленькие: диаметром 5 мм и весом 0,5 г. Их легко не заметить во время операции и удалить вместе с щитовидной железой. К тому же, даже если сохранить эти железы, высока вероятность повреждения питающих их кровеносных сосудов и нервов. А значит, железы просто перестанут работать, и в организм перестанет поступать паратиреиодный гормон. Это чревато возникновением тетанических приступов (подергиваний, которые могут переходит в судороги), нарушением питания волос и ногтей, кожи, эмали зубов, а также отложением кальция вне костей, например, между нервными клетками, что может проявляться в виде паркинсонизма или хореоатетоза — комбинации быстрых порывистых движений с медленными судорожными.
- Повреждение возвратного гортанного нерва и парез гортани. Щитовидная железа располагается прямо перед гортанью. Там же рядом находятся голосовые связки. Все эти структуры иннервируются гортанными нервами. И в случае повреждение некоторых из них — возвратных гортанных нервов — у пациента будет наблюдаться уменьшение активности гортанных мышц, что влечет за собой проблемы работы голосовых связок (в основном, осиплость голоса) и нарушения функций дыхания.
Согласитесь, последствия не из приятных. Поэтому главный вопрос заключается в следующем: оправдывают ли риски тиреоидэктомии ее пользу? На данном этапе развития науки и медицины нельзя дать однозначный ответ. Но важно понимать, что диагноз «Рак щитовидной железы» ничего не говорит о прогнозе для пациента и смертность от него крайне низка. А вот неоправданное агрессивное лечение, а именно удаление щитовидной железы, может повлечь за собой инвалидизацию и значительное ухудшение качества жизни. Поэтому сейчас в научном сообществе наблюдается тенденция органосохраняющей тактики в отношении высокодифференцированных РЩЖ. А показания к УЗИ щитовидной железы касаются только специфических групп пациентов. Ведь обнаружение раковых клеток в организме не означает смерть, а вот риск невротизации значительно возрастает.
Какой существует выход?
Одним из наиболее перспективных выходов из ситуации является частичное удаление ткани ЩЖ, а именно поврежденной доли. В таком случае пациент, во-первых, избавляется от необходимости принимать пожизненную заместительную терапию гормонами щитовидной железы, а во-вторых, избегает тех серьезных последствий, которые несет за собой операция полного удаления ЩЖ. Однако стоит понимать, что такой вариант не касается опухолей большого размера, а также тех новообразований, которые потенциально могут быть агрессивными (это решает врач!).
Сейчас терапевты и хирурги, которые занимаются патологией щитовидной железы, разделились на два лагеря: те, кто считает, что лучше перестраховаться, и при выявлении даже самой маленькой опухоли удалить всю щитовидную железу, и те, кто считает, что лучшим выходом будет частичное удаление ткани железы, а именно поврежденной ее доли. К сожалению, этот вопрос до сих пор остается открытым. Врачи все еще не могут прийти к единому знаменателю в данном вопросе. Проблема в том, что достоверная объективная доказательная база, на которую врачи могли бы опираться в качестве актуального клинического руководства, вовсе отсутствует. Существуют лишь отдельные исследования, которые обозревают вопрос лишь с одной субъективной стороны [21]. Оптимальным решением данной проблемы, на наш взгляд, стало бы объединение всех существующих статей с объективным и всесторонним взглядом на этот вопрос. Однако подобное исследование лишь ожидает нас в будущем.
Финальный аккорд
Итак, вот мы и подошли к последним строкам нашей статьи. Могло показаться, что мы и вовсе против УЗИ щитовидной железы, однако это не так. Существует группа риска пациентов, которым необходимо сделать УЗИ щитовидки (например, РЩЖ у кого-то из членов семьи). Также нельзя игнорировать тот факт, что УЗИ сильно продвинуло врачей в ранней диагностике агрессивных быстротекущих форм РЩЖ. Однако бóльшая часть врачей-эндокринологов, особенно за границей, против того, чтобы делать УЗИ щитовидки тогда, когда нет никаких симптомов болезни! Необходимой к прочтению, на наш взгляд, является работа профессора Фадеева В.В. «На всякий случай…» [28].
В этой статье высококвалифицированный врач обращает внимание читателя на то, что часто врачи оценивают результаты лабораторных и инструментальных анализов только на основании общепринятых границ норм. В случае несоответствия данной «норме» пациент признается больным. Очень важно понимать, что человек — индивидуальность, и показатель нормы у каждого может варьировать в зависимости от особенностей организма. Поэтому и лечить мы должны не анализы, не болезнь, а пациента. Врачу необходимо оценивать не только цифры в листе анализов, но и состояние пациента, а также качество жизни, которое ждет человека после лечения. Это и называется клиническим мышлением, которое, к сожалению, зачастую отсутствует у врачей в век, когда мы хотим слепо довериться цифрам, а машина начинает думать за человека.
С этими и другими мыслями вы можете ознакомится по оставленной нами ссылке [26].
Итак, дорогие наши читатели! Опираясь на всё, о чем мы рассказали выше, мы бы хотели, чтобы вы сделали три главных вывода:
- Не делайте УЗИ щитовидной железы «на всякий случай», без каких-либо симптомов! Ни по совету подруги, ни потому, что так сказали по телевизору, ни даже если вам сказал так врач (только если он четко объяснит, зачем нужно делать УЗИ).
- Если у вас нашли узел — 90%, что он доброкачественный.
- Если вы попали в оставшиеся 10%, помните, что бóльшая часть РЩЖ хорошо поддается лечению и имеет благоприятный прогноз.
Всем хорошего дня, и берегите свои щитовидки и нервы.
- Циберкин А. (2019). Всегда ли нужна биопсия узлов щитовидной железы? «Медфронт»;
- Carolyn Dacey Seib, Julie Ann Sosa. (2019). Evolving Understanding of the Epidemiology of Thyroid Cancer. Endocrinology and Metabolism Clinics of North America. 48, 23-35;
- Hyeong Sik Ahn, Hyun Jung Kim, H. Gilbert Welch. (2014). Korea’s Thyroid-Cancer “Epidemic” — Screening and Overdiagnosis. N Engl J Med. 371, 1765-1767;
- Yasuhiro Ito, Akira Miyauchi, Minoru Kihara, Takuya Higashiyama, Kaoru Kobayashi, Akihiro Miya. (2014). Patient Age Is Significantly Related to the Progression of Papillary Microcarcinoma of the Thyroid Under Observation. Thyroid. 24, 27-34;
- S. Suzuki. (2016). Childhood and Adolescent Thyroid Cancer in Fukushima after the Fukushima Daiichi Nuclear Power Plant Accident: 5 Years On. Clinical Oncology. 28, 263-271;
- Alexandria D. McDow, Susan C. Pitt. (2019). Extent of Surgery for Low-Risk Differentiated Thyroid Cancer. Surgical Clinics of North America. 99, 599-610;
- Toru Takano. (2017). Natural history of thyroid cancer [Review]. Endocr J. 64, 237-244;
- Noone A.M., Howlader N., Krapcho M., Miller D., Brest A., Yu M. et al. SEER cancer statistics review, 1975-2015. Bethesda: National Cancer Institute, 2018;
- A. Kurjak. (2000). Ultrasound scanning – Prof. Ian Donald (1910–1987). European Journal of Obstetrics & Gynecology and Reproductive Biology. 90, 187-189;
- Ian Donald, R.E. Steiner. (1953). RADIOGRAPHY IN THE DIAGNOSIS OF HYALINE MEMBRANE. The Lancet. 262, 846-849;
- Louise Davies, H. Gilbert Welch. (2014). Current Thyroid Cancer Trends in the United States. JAMA Otolaryngol Head Neck Surg. 140, 317;
- Hyeyeun Lim, Susan S. Devesa, Julie A. Sosa, David Check, Cari M. Kitahara. (2017). Trends in Thyroid Cancer Incidence and Mortality in the United States, 1974-2013. JAMA. 317, 1338;
- Antonino Belfiore, Dario Giuffrida, Giacomo L. La Rosa, Orazio Ippolito, Giovanna Russo, et. al.. (1989). High frequency of cancer in cold thyroid nodules occurring at young age. Acta Endocrinologica. 121, 197-202;
- S. Ezzat. (1994). Thyroid incidentalomas. Prevalence by palpation and ultrasonography. Archives of Internal Medicine. 154, 1838-1840;
- Carolyn Dacey Seib, Julie Ann Sosa. (2019). Evolving Understanding of the Epidemiology of Thyroid Cancer. Endocrinology and Metabolism Clinics of North America. 48, 23-35;
- Hyeong Sik Ahn, H. Gilbert Welch. (2015). South Korea’s Thyroid-Cancer “Epidemic” — Turning the Tide. N Engl J Med. 373, 2389-2390;
- Louise Davies, H. Gilbert Welch. (2006). Increasing Incidence of Thyroid Cancer in the United States, 1973-2002. JAMA. 295, 2164;
- A.T. Grady, J.A. Sosa, T.P. Tanpitukpongse, K.R. Choudhury, R.T. Gupta, J.K. Hoang. (2015). Radiology Reports for Incidental Thyroid Nodules on CT and MRI: High Variability across Subspecialties. AJNR Am J Neuroradiol. 36, 397-402;
- Hirsch E.F. (1947). Unnecessary operations. Ill. Med. J. 5;
- Horwitz A. (1947). Unnecessary surgery. Med. Ann. Dist. Columbia. 11, 605–608;
- H. Gilbert Welch, Gerard M. Doherty. (2018). Saving Thyroids — Overtreatment of Small Papillary Cancers. N Engl J Med. 379, 310-312;
- Akira Miyauchi, Yasuhiro Ito, Hitomi Oda. (2018). Insights into the Management of Papillary Microcarcinoma of the Thyroid. Thyroid. 28, 23-31;
- Iwao Sugitani, Kazuhisa Toda, Keiko Yamada, Noriko Yamamoto, Motoko Ikenaga, Yoshihide Fujimoto. (2010). Three Distinctly Different Kinds of Papillary Thyroid Microcarcinoma should be Recognized: Our Treatment Strategies and Outcomes. World J Surg. 34, 1222-1231;
- Benjamin R. Roman, Luc G. Morris, Louise Davies. (2017). The thyroid cancer epidemic, 2017 perspective. Current Opinion in Endocrinology & Diabetes and Obesity. 24, 332-336;
- Brooke Nickel, Caitlin Semsarian, Ray Moynihan, Alexandra Barratt, Susan Jordan, et. al.. (2019). Public perceptions of changing the terminology for low-risk thyroid cancer: a qualitative focus group study. BMJ Open. 9, e025820;
- Дедов И.И. и Мельниченко Г.А. Эндокринология: национальное руководство (2-е изд.). М.: «ГЭОТАР-Медиа», 2019. — 1112 с.;
- Дедов И.И., Мельниченко Г.А., Фадеев В.В. Эндокринология: учебник (3-е изд.). М.: «Литтерра», 2015. — 416 с.;
- Фадеев В.В. (2017). На всякий случай… «Клиническая и экспериментальная тиреоидология». 2.
Биопсия — самый «близкий к телу» метод диагностики. От пациента отщипывают кусочек и изучают под микроскопом. В воображении некоторых пациентов биопсия приравнивается чуть ли не к хирургической операции. Это не так, хотя и то, и другое может проводиться одновременно. Что же такое биопсия, какая она бывает и для чего проводится, рассказывает MedAboutMe.
Что такое биопсия в медицине?
Биопсия — это метод анализа тканей человеческого организма. Суть его очень проста: взять образец органа (биоптат), извлечь его из организма и внимательно рассмотреть. Собственно, сам термин это и означает в переводе с греческого: bios — живой и opsis — наблюдение при помощи глаз, то есть, визуальное исследование живой ткани.
История биопсии начинается с имени арабского врача Альбукасиса, которого называют мусульманским отцом хирургии — он же Абу аль-Касим Аль-Захрави. Именно он впервые использовал полую иглу, чтобы получить образец тканей зоба щитовидной железы и впоследствии исследовать его. Долгое время врачи делали биопсию, скорее, случайно, чем намеренно. Но в конце XIX века все изменилось. Технологии исследования тканей при помощи микроскопа и возможности взятия образцов развились достаточно — и медицина получила новый метод.
В России первую диагностику при помощи биопсии провел в 1875 году доктор М.М. Руднев. В 1878 году немецкие ученые описали исследование образца шейки матки. А в 1879 году парижский дерматолог Эрнест Анри Бенье, который проводил научные изыскания в области болезней кожи, ввел термин «биопсия», обозначив им процедуру взятия образцов тканей.
Следует понимать, что биопсия — это инвазивный метод, то есть, при этом совершается проникновение в тело человека. И это травматичный метод, приводящий хоть и к минимальным, но повреждениям тканей. Поэтому врачи назначают биопсию тогда, когда без нее не обойтись. Просто так данный метод никогда не используется.
Итак, биопсия позволяет получить образец клеток или тканей. Его можно изучать на клеточном уровне, то есть, исследуется состояние отдельных клеток и их компонентов — цитологическое исследование, для которого может использоваться световой или более мощный, электронный микроскоп. А можно при помощи светового микроскопа анализировать срез ткани — при многих заболеваниях изменения происходят в структуре ткани органа. Иногда при проведении гистологического анализа требуется предварительная обработка образцов специальными растворами — их окрашивание или иная подготовка для диагностики.
В зависимости от того, какой метод предполагается использовать, биопсия проводится разными путями.

Как получить образец для исследования при биопсии?

Для цитологического исследования образцы материала получают одним из следующих методов:
- Соскоб (мазок) — с пораженных тканей специальным шпателем или скальпелем на предметное стекло соскребается некоторое количество материала.
- Тонкоигольная биопсия — клетки органа или жидкость забираются путем отсасывания через полую длинную тонкую иглу. Так получают образцы костного мозга или кист.
При заборе кусочка тканей, в зависимости от того, какие ткани и каким образом надо исследовать, выделяют два вида биопсии:
- Эксцизионная — при этом удаляется и направляется на исследование все образование, а не отдельная его часть. Например, это может быть подозрительная родинка. В этом случае биопсия является одновременно и лечебной, и диагностической процедурой: сначала подозрительные ткани полностью удаляют, а потом проверяют: насколько они были опасны и не стоит ли поискать другие проявления болезни.
- Инцизионная — на исследование забирается только часть пораженной болезнью ткани.
Забор тканей может проводиться разными путями:
- Пункционная биопсия — образец тканей забирается при помощи полой иглы. Обычно используется для получения образца тканей, расположенных недалеко от поверхности кожи.
- Трепан-биопсия позволяет получать образец ткани в виде столбика при помощи трепана — специальной полой трубки. Используется при необходимости получения образца из плотных опухолей и костей.
- Кор-биопсия (режущая, сердцевинная биопсия) — разновидность трепан-биопсии, отличающаяся от нее механическими особенностями трепана. Проводится при помощи биопсийного пистолета — устройства для получения образцов молочной и щитовидной желез, почек, простаты, печени и других мягких тканей.
- Петлевая биопсия — при этом образец забирается при использовании петли и устройства, позволяющего резать ткань (коагулятор или радиочастотный аппарат). Проводят при эндоскопических исследованиях, а также при гинекологическом обследовании и др.
- Щипковая биопсия (панч-биопсия) — образец ткани удается получить при помощи специальных щипцов. Чаще всего используется при заболеваниях пищевод, желудка и кишечника.
- Скарификационная биопсия проводится устройством, позволяющим срезать тонкий слой ткани. Обычно используется при необходимости проведения биопсии кожи.
Самый частый побочный эффект биопсии — боль при проведении процедуры. Поэтому в большинстве случаев предварительно проводится местная анестезия — обезболивание конкретного участка, на котором будет проводиться забор тканей. Но, если речь идет только о соскобе, то, конечно, анестезия не нужна.
Биопсия не проводится при нарушениях свертываемости крови, а также при возможности получить требуемые данные другими, неинвазивными методами диагностики.
Биопсия и диагностика заболеваний

Устоялось мнение, что биопсия проводится, прежде всего, для опровержения или подтверждения предварительного диагноза «рак». И действительно, этот метод обязателен для окончательной постановки диагноза онкологами. Но он также успешно применяется и в других направлениях медицины, а не только в онкологии.
- Урологи исследуют ткани мочеполовой и мочевыделительных систем для поиска воспалительных процессов почек и мочевого пузыря, а также кистозных образований в них;
- Гинекологи при помощи биопсии диагностируют бесплодие, воспаление, предраковые состояния, а также некоторые эндокринные болезни;
- Гастроэнтерологи анализируют состояние желудочно-кишечного тракта: выявляют участки воспаления и ткани в предраковом состоянии и др.;
- Пункция лимфатических узлов проводится для их оценки при аутоиммунных, инфекционных и онкологических заболеваниях.
- Биопсия пересаженных органов необходима, чтобы проверить, не идет ли реакция отторжения.
- Пункция спермы может проводиться для оценки фертильности в ходе лечения бесплодия.
А в феврале этого года американские ученые сообщили, что разработали метод ранней диагностики болезни Паркинсона путем биопсии тканей подчелюстной слюнной железы. Метод позволяет выявить белок, указывающий на наличие болезни, на стадии, когда нет даже первых признаков заболевания. Это значит, что можно будет раньше начать лечение.
Обычно биопсия назначается, когда нет других возможностей получить информацию о клетках и тканях пораженного органа. Причем нередко забор тканей проводится «заодно» — раз уж все равно добрались до больного органа, почему бы не отщипнуть кусочек для анализа. То есть, взять образец тканей можно в процессе хирургической операции или других диагностических процедур, таких как:
- эндоскопия,
- колоноскопия,
- бронхоскопия и др.
Для проведения биопсии врач может воспользоваться дополнительным оборудованием, позволяющим наблюдать за процедурой, чтобы «не промахнуться» — томографом, аппаратом УЗИ или иной аппаратурой.
Ошибки при проведении биопсии

Идеальных методов диагностики медицина не знает. При проведении биопсии тоже возможны ошибки и получение ложноотрицательного результата, то есть, болезнь есть, но ее не нашли. Так, считается, что гистологическое исследование тканей — довольно точный метод и достоверен на 90%. Что может быть причиной ошибок при биопсии:
- при заборе было получено слишком мало материала и его оказалось недостаточно для полноценной диагностики;
- забор материала для анализа произведен не из опухоли, а из здоровых тканей рядом с ней;
- материал взят из зоны фиброза или некроза опухоли и не дает достаточно информации, чтобы определить наличие злокачественного образования;
- при подготовке материала к исследованию срез был проведен под неудачным углом;
- врач-морфолог не обладал достаточным опытом для выявления характерных признаков на сложном образце.
Выводы
- Биопсия — инвазивный, но малотравматичный метод диагностики, который никогда не назначается врачом просто так, без достаточных на то оснований. Если врач считает, что нужна биопсия — лучше не спорить, часто вовремя проведенный анализ является залогом жизни пациента.
- Современные технологии позволяют провести биопсию качественно и практически безболезненно.
- Результаты биопсии считаются окончательными. По ним врач может назначать лечение. Если результаты вызывают сомнения у врача (например, по всем признакам есть опухоль, а биопсия ее не показала) — возможна ошибка при заборе пробы. В этом случае врач может направить пациента на повторный анализ.
- Если результаты биопсии вызывают сомнения у пациента, он может забрать свои «стекла» с гистологическими срезами и отправить их на повторный анализ в другую клинику.
Клиническая лабораторная диагностика: национальное руководство / Под ред. В. В. Долгова, В. В. Меньшикова. – 2012
Руководство по лабораторным методам диагностики / Кишкун А.А. – 2013
Диагностика заболеваний редко обходится без инструментальных и лабораторных исследований. Оценки симптомов недостаточно — нужно узнать, что происходит внутри органов и тканей. Одним из наиболее точных методов обследования является биопсия. Врач производит забор тканевого материала в области предполагаемого патологического процесса с целью его дальнейшего изучения. Микроскопический анализ полученного образца помогает выявить характерные для определенного заболевания изменения. В онкологической практике биопсия считается информативным методом уточнения типа опухоли, ее стадирования.

- Что это за анализ?
- Показания к проведению
- Виды и способы проведения биопсии
- Подготовка
- Может ли биопсия быть ошибочной?
Что это за анализ?
Биопсия — высокоинформативный способ обследования, применяемый в случае необходимости анализа клеток в определенной анатомической области. Забор тканей с их последующим обследованием с помощью микроскопии дает возможность точно оценить клеточный состав. Без такой процедуры сложно обойтись, если врач подозревает наличие доброкачественного или злокачественного новообразования в определенном органе. Это уточняющее исследование, дополняющее результаты других диагностических процедур. Онколог анализирует результаты биопсии, рентгенографии, эндоскопии и иммунологических тестов совместно.
Онкологические заболевания развиваются быстро и угрожают жизни пациента. Нужно как можно раньше выбрать наиболее эффективную схему лечения. Именно с этой целью проводится биопсия. По результатам процедуры врач приходит к выводу, какие травматичные или даже опасные с точки зрения осложнений способы лечения уместны в данном случае. Подбирается тактика оперативного вмешательства, радиотерапии, химиотерапевтического лечения. Все это было бы невозможно без точного определения типа опухоли, ее стадии и распространенности в организме. Нужны цитологические и гистологические тесты.
В качестве примера можно привести злокачественное новообразование прямой кишки, растущее в нижней части органа. В качестве основного метода лечения выполняется иссечение этой анатомической структуры с последующим формированием колостомы для выделения каловых масс. Если диагноз не был полностью подтвержден, подобное вмешательство не проводят. Оно может по ошибке сделать пациента инвалидом.

Показания к проведению
Подобная диагностическая процедура требуется, если врач предполагает о наличии патологического процесса, подтверждение которого невозможно с помощью других способов исследования. В большинстве случаев это онкологические болезни, однако область применения биопсии ими не ограничивается. Например, такое исследование часто назначают гастроэнтерологи для оценки состояния слизистой оболочки органов пищеварительного тракта. Определяется вид воспалительного процесса, подбирается способ его лечения. В гинекологии и эндокринологии этот метод дает возможность определить причину нарушения фертильности, обнаружить ранние признаки воспаления и дисплазии.
Также биопсия необходима для определения особенностей течения и степени тяжести патологического процесса при болезнях печеночной ткани, почек, головного мозга, мышц и других анатомических структур. Это важно для подбора и изменения схемы медикаментозной терапии. По результатам анализа врач определяет прогностические данные.
Виды и способы проведения биопсии
В современной клинической практике чаще всего используют следующие методики выполнения биопсии:
- Мазки, соскобы и бритвенный метод. Зачастую специалисту требуется небольшое количество материала для постановки диагноза. Можно выполнить мазок и получить все необходимые данные при его последующей микроскопии. Например, такой способ часто применяют в гинекологии. Бритвенная биопсия предполагает иссечение тонкого участка кожного покрова с помощью скальпеля или другого инструмента.
- Тонкоигольная пункция. Такая процедура тоже подходит для случаев, когда достаточно получить немного клеток. В область предполагаемого патологического процесса вводится тонкая игла, захватывающая тканевой образец.
- Толстоигольная пункция. Позволяет произвести забор большого образца тканей без иссечения. Ее назначают при злокачественном новообразовании молочной железы, печеночной ткани, предстательной железы. Трепан-биопсия подходит для исследования кожного покрова, костномозговых структур. Используется специальный инструмент в форме цилиндра.
- Аспирационный метод. Это современная техника забора материала, при котором используется вакуумный прибор в форме цилиндра. В качестве механизма применяется отрицательное давление. Прибор присоединяют к игле. Аспирация дает возможность взять несколько образцов в разных участках анатомической структуры.
- Операционная биопсия. Проводится непосредственно во время операции, когда врач иссекает опухолевую ткань. Это высокоинформативное исследование, позволяющее оценить состояние большого количества тканей. Минус такого вида процедуры — определить тип болезни можно только после операции. Плюсом можно считать совмещение лечебной практики с достоверной диагностикой.
- Эндоскопическая биопсия. Проводится во время диагностики внутренних полостных структур, вроде пищеварительного или респираторного тракта. С помощью эндоскопа врач осматривает подозрительные участки тканей и выбирает место забора материала. Плюсом такой техники можно считать повышенную точность результатов исследования.
Способ проведения диагностики выбирают в зависимости от анамнеза пациента.

Подготовка
В большинстве случаев специально готовиться не следует. Достаточно прийти к врачу в день проведения процедуры и подписать необходимые документы. Специалист объяснит, как будет проходить обследование. Расскажет о рисках и возможных неприятных ощущениях. Определенные виды биопсии выполняют под местным обезболиванием. Реже требуется наркоз. Пациент может сам выбирать комфортный для него способ выполнения диагностики. В случае наркоза нужны специальные подготовительные процедуры.
Для биопсии характерны стандартные осложнения, возникающие при других видах вмешательств. Возможно кровоизлияние, инфицирование тканей. Реже возникает травматизация внутренних органов. Такие негативные последствия редки, но врач обязательно уведомляет пациента о рисках.

Может ли биопсия быть ошибочной?
Достоверность исследования зависит от способа его проведения, анамнеза пациента, опыта врача и других факторов. Например, при пункции специалист может получить образец тканей без злокачественных клеток, если игла попала в соседнюю с опухолью область. В этом случае возможен ложноположительный результат. Онкологи учитывают такую вероятность, и всегда назначают уточняющие исследования. Диагноз не ставится только на основе результатов одной процедуры. Всегда проводится комплексная оценка состояния организма.


Содержание:
- Показания и противопоказания к пункции щитовидной железы
- Подготовка и техника проведения пункции щитовидной железы
- Лабораторный этап исследования и его результаты
- Варианты заключений цитолога
Патология щитовидной железы довольно распространена, особенно, в некоторых географических зонах, а по данным статистики, к 50-летию примерно половина женского населения планеты «обзаводится» узлами в органе. С увеличением возраста растет и этот показатель, и к 70 годам узлы можно обнаружить практически у всех. Такая ситуация требует от врачей не только своевременной диагностики патологического процесса и исключения рака, но и дифференцированного подхода в отношении необходимости операции.
Пункция щитовидной железы с последующим цитологическим исследованием ее ткани считается едва ли не самым важным методом диагностики заболеваний органа. Раньше основное значение имело УЗИ, однако оно не дает абсолютной точности, возможны ошибочные выводы и, соответственно, неправильная тактика ведения, поэтому тонкоигольная биопсия под контролем УЗИ — «золотой стандарт» при обследовании больных, имеющих ту или иную патологию.
Результат пункции диктует врачу дальнейшую тактику ведения пациента — оперировать, наблюдать или лечить консервативно, ведь не зная точно, какое строение имеет образование в паренхиме органа, эндокринолог рискует ошибиться, а последствия окажутся плачевными для больного.
Многие считают, что раз назначена пункция, то впереди обязательно ждет и операция. Однако это не совсем так. Действительно, еще совсем недавно хирурги придерживались активной тактики для большинства пациентов с узлами в органе, но появление высокоинформативных способов диагностики и исключения рака позволило значительно снизить число необоснованно прооперированных.
Учитывая данные статистики относительно распространенности узлообразования в щитовидной железе и проводя всем без исключения удаление и узлов, и органа, хирурги оставили бы без щитовидной железы практически всех людей пожилого возраста. Понятно, что оправданным такой подход считать нельзя, ведь операция имеет ряд осложнений — нарушение голоса, расстройства кальциевого обмена и т. д. Кроме того, хирургия — это еще и весьма затратная сфера в системе здравоохранения, и чем больше операций проводится необоснованно, тем выше и бесполезные траты бюджетных средств.
Таким образом, пункция щитовидной железы позволяет ответить на несколько важнейших вопросов: злокачественный или доброкачественный характер несет в себе узел щитовидной железы, есть ли показания к оперативному лечению, каков должен быть его объем.
Применение пункции показало, что лишь около 5% всех узловых образований щитовидной железы являются злокачественными, остальные — «добрые», не имеющие склонности малигнизироваться. Точное определение показаний к операции снизило число прооперированных больных почти в десять раз, но среди тех, кому удалили орган, значительно возросло количество случаев рака. Это говорит о том, что операции после внедрения пункционной биопсии стали проводиться тем, кому они действительно нужны.
Роль пункционной биопсии в диагностике патологии щитовидной железы сложно переоценить. Благодаря своей информативности, метод успешно применяется во всех эндокринологических клиниках, он прост в исполнении, не требует дорогостоящего оснащения и хорошо переносится большинством пациентов.
Показания и противопоказания к пункции щитовидной железы

Если ранее считалось, что проведение пункционной биопсии показано всем пациентам с наличием узла в щитовидной железе более 1 см в диаметре, то в настоящее время показания к ее проведению многими профильными организациями во всем мире ограничиваются. Так в России с недавних пор применяется система сонографической оценки стратификации риска злокачественности узлового образования щитовидной железы EU TIRADS, согласно которой для определения показаний к проведению биопсии учитывается сонографическая структура и размеры узлового образования.
Алгоритм EU-TIRADS для стратификации риска злокачественных новообразований и принятия решения о ТАБ.

Согласно системе EU TIRADS пункционная биопсия узлов, которые являются со 100% вероятностью доброкачественными (простые кисты и губчатые (спонгиформные) узлы) можно не пунктировать.


Узлы, которые согласно системе EU-TIRADS имеют низкий риск злокачественности (EU-TIRADS-III) – 2-4% (овальные, с ровным краем, изоэхогенные/гиперэхогенные солидные узлы) подлежат пункционной биопсии при размере узла более 2 см в диаметре.


Узлы, имеющие средний (промежуточный) риск злокачественности (овальные, с ровным краем, слегка гипоэхогенные узлы) (EU-TIRADS IV) – 6-17%, необходимо пунктировать при размерах более 1,5 см в диаметре.

А вот узлы, имеющие высокий риск злокачественности (EU-TIRADS V) подлежат пункционной биопсии при размере 1 см в диаметре. К таким узлам относятся узловые образования, имеющие хотя бы один из больших признаков злокачественности:
- неправильная форма
- неровный край
- микрокальцинаты
- выраженная (по отношению к претиреоидным мышцам) гипоэхогенность
Риск злокачественности таких узлов составляет 26-87%!




Как правило, такие узлы лучше пропунктировать из 2-3 точек.
Повторная биопсия может быть показана в случае, когда первоначально доброкачественный процесс начинает вести себя подозрительно в отношении рака — появляется бугристость контуров, в паренхиме на УЗИ видны кальцинаты, а на шее прощупываются увеличенные лимфатические узлы.
Также пациенту могут назначить повторное исследование, если первая биопсия была проведена не в специализированном медицинском центре либо при исследовании были допущены ошибки, неточность в формулировках, материал оказался неинформативным и т. д.
Противопоказаний к тонкоигольной пункционной биопсии щитовидной железы практически нет. Метод считается безопасным для абсолютного большинства больных. Однако сложности могут возникнуть при обследовании детей младшего возраста, лиц с психическими отклонениями, которым может быть показан кратковременный общий наркоз на время исследования. В случае гипертонических кризов, аритмий и других сердечно-сосудистых нарушений вопрос о безопасности и времени проведения процедуры решается индивидуально.
Подготовка и техника проведения пункции щитовидной железы
Забор биопсийного материала из щитовидной железы проводится амбулаторно и занимает около четверти часа. Большая часть времени уходит на укладывание пациента, оформление документации, объяснение сути манипуляции, в то время как сам прокол и получение ткани — это считанные минуты.
 Какой-либо специальной подготовки перед пункцией не требуется. Больной может вести привычный образ жизни, пить и есть накануне исследования. Принимаемая пища не окажет влияния на результат, узел не изменит от нее своего строения, однако чувствительные и эмоциональные люди могут испытывать тошноту, головокружения и даже падать в обморок, поэтому лучше все же на нагружать свой желудок чрезмерно, но и отказываться от еды недопустимо, ведь обморок может наступить и у проголодавшихся пациентов.
Какой-либо специальной подготовки перед пункцией не требуется. Больной может вести привычный образ жизни, пить и есть накануне исследования. Принимаемая пища не окажет влияния на результат, узел не изменит от нее своего строения, однако чувствительные и эмоциональные люди могут испытывать тошноту, головокружения и даже падать в обморок, поэтому лучше все же на нагружать свой желудок чрезмерно, но и отказываться от еды недопустимо, ведь обморок может наступить и у проголодавшихся пациентов.
Немаловажно подготовиться к процедуре и психологически, ведь излишний страх не только не оправдан, но и мешает самому пациенту объективно оценивать свое самочувствие. Возможная боль — основная причина страха. Учитывая, что укол производится в шею, он еще больше усиливается.
Многие пациенты боятся пункции и начинают паниковать заранее, думая, что это больно и крайне неприятно, а в последствии их непременно ждет операция. Однако, им можно успокоиться: применение тонких игл и, при необходимости, местных анестетиков делает пункцию почти безболезненной. Ощущения от нее сродни тем, которые все мы испытывали не раз при внутримышечных инъекциях, то есть вполне терпимы.
Другим поводом для беспокойства может стать опасение, что хирург попадет иглой не туда, куда нужно, либо спровоцирует прогрессирование патологии. Об этом не стоит беспокоиться, учитывая, что все пункции проводятся под контролем ультразвукового датчика, а после процедуры не происходит ускорения роста узлов или распространения опухоли за пределы органа.
Современные стандарты пункции щитовидной железы требует проведения процедуры только под контролем УЗИ. Дополнительная визуализация органа и объемных образований в нем повышает точность прокола до 100%, исключает взятие ткани из другого участка, позволяет сделать пункцию в наиболее измененной области узла.
Большинство больных не нуждаются в анестезии, поскольку прокол осуществляется крайне быстро, и тонкая игла практически не травмирует железу. Показания к операции зависят от результата цитологии, и необходима она далеко не каждому.
Особо чувствительным и эмоциональным субъектам может быть проведено местное обезболивание специальными кремами или спреями с анестетиком, что не снижает эффективности процедуры, но облегчает ее проведение для конкретного обследуемого.
Берут пункцию при помощи тонких игл, и чем меньше ее диаметр, тем лучше: больной меньше ощущает момент прокола, а врач получает более качественный материал, не смешанный с кровью в связи с малой травматичностью.
 Пункция узла щитовидной железы проводится в процедурном кабинете и всегда под контролем ультразвука. Она включает несколько этапов:
Пункция узла щитовидной железы проводится в процедурном кабинете и всегда под контролем ультразвука. Она включает несколько этапов:
- Укладывание обследуемого на спину, под которую помещается валик или подушка, помогающая достичь максимального разгибания шейного отдела и облегчения доступа к железе;
- Поиск с помощью ультразвука узлового образования в паренхиме органа, уточнение его локализации и размеров, наличия дополнительных включений (кальцинаты, рубцы, кисты);
- Обработка кожи в месте прокола антисептическими средствами, ограничение зоны манипуляции стерильными салфетками;
- Введение пункционной иглы быстрым, но аккуратным движением в требуемую область под контролем УЗИ, забор материала для исследования;
- Извлечение иглы наружу и помещение полученной ткани на предметное стекло, которое после будет подвергнуто микроскопии.
Когда игла достигла узлового образования, хирург четко видит ее на экране аппарата УЗИ, продвигая в самый подозрительный участок патологического очага. По мере всасывания шприцем ткани хирург перемещает иглу в разных направлениях, стремясь изъять из органа как можно более разнообразный клеточный субстрат.
Цитологический мазок, полученный на предметном стекле, направляется на исследование к врачам-цитологам, которые помогут с определением окончательного диагноза. Заключение пациент получит в течение недели после исследования, в зависимости от сложности клинического случая и загруженности цитологической лаборатории.
Место прокола после извлечения иглы заклеивается лейкопластырем, и уже через 10-15 минут в случае хорошего самочувствия пациент может отправиться по своим делам. В день процедуры разрешается принимать душ, заниматься спортом, есть и пить в привычном режиме.
Пункция щитовидной железы считается безопасной и практически безболезненной процедурой и, вместе с тем, высокоинформативным и незаменимым этапом диагностического поиска. Осложнения при ней крайне редки, хотя исключить их полностью все же нельзя. Наиболее вероятными последствиями могут стать небольшая гематома в месте прокола кожи, что не представляет угрозы здоровью обследуемого, а также обмороки в момент забора ткани, которые более часты у эмоционально лабильных и чрезмерно боящихся исследования пациентов.
Лабораторный этап исследования и его результаты
Все пациенты, прошедшие пункцию щитовидной железы, хотят получить не только быстрый, но и максимально точный цитологический диагноз. Этого же желают и врачи, однако на деле случается иначе. Заключения могут быть не информативными, если в материале не было клеток, а содержался коллоид, если обнаружены признаки аутоиммунного тиреоидита, но ничего не сказано о характере опухолевидного образования и т. д.
Как показывает практика, вероятность получения точного цитологического ответа прямо связана с опытом хирурга, проводившего пункцию. Чем прицельнее он взял ткань для исследования, тем выше вероятность достоверного и развернутого вывода о характере патологии. Считается, что доля неинформативных ответов минимальна у специалиста, который проводит не менее 40 биопсий в неделю, а в крупных эндокринологических центрах этот показатель достигает нескольких сотен.
 Для повышения информативности и предупреждения повторных пункций в настоящее время проводится исследование пунктата из узла щитовидной железы методом жидкостной цитологии. В этом случае пунктат помещается не на предметное стекло, а в специальную емкость с жидкостью (виал). Далее, путем центрифугирования этой жидкости, происходит отделение клеток щитовидной железы от клеток крови и коллоида. В результате этого цитолог может более точно определиться с природой узлового образования щитовидной железы.
Для повышения информативности и предупреждения повторных пункций в настоящее время проводится исследование пунктата из узла щитовидной железы методом жидкостной цитологии. В этом случае пунктат помещается не на предметное стекло, а в специальную емкость с жидкостью (виал). Далее, путем центрифугирования этой жидкости, происходит отделение клеток щитовидной железы от клеток крови и коллоида. В результате этого цитолог может более точно определиться с природой узлового образования щитовидной железы.
Когда пациент уже покинул клинику, начинается наиболее сложный и ответственный этап всей морфологической диагностики. Стекла с мазками ткани железы просушиваются и отправляются в цитологическую лабораторию, где производится их окрашивание методиками Май-Грюнвальд-Гимзы или Папаниколау. Клетки исследуются микроскопически врачом-цитологом.
Морфологические особенности пунктата — строение клеток, их размеры, включения в цитоплазме, атипия — предопределяют диагноз, который в дальнейшем будет решающим при выборе лечебной тактики.
У 9 из 10 пациентов цитолог может сформулировать предельно точный диагноз, но случается, что данных микроскопии недостаточно для исключения или подтверждения злокачественности опухолеподобного процесса (много крови в пунктате, низкая клеточность ввиду плотности узла и др.).
Причиной неинформативности могут стать не только техническая погрешность при проведении процедуры или недостаточный опыт хирурга, но и слишком разнообразный клеточный состав, когда даже очень грамотному цитологу сложно выделить преобладающий тип клеток. В этом случае специалисту ничего не остается, как констатировать неинформативность материала и порекомендовать повторную пункцию железы.
В ожидании результатов исследования, пациенты очень волнуются, ведь главная задача хирурга и цитолога — исключить злокачественную опухоль. В среднем время ожидания результата занимает около недели, хотя само приготовление препаратов и их просмотр возможны в течение одного дня.
Крупные центры, специализирующиеся на патологии щитовидной железы, выдают заключения через 1-2 дня, так как штат специалистов позволяет провести диагностику максимально быстро даже при высокой загруженности пациентами. Это позволяет минимизировать стресс у больных в ожидании ответа без ущерба качеству исследования.
Пациенту на руки выдается заключение с результатом исследования, в котором указана не только цитологическая картина (главная цель пункции), но и точные размеры и расположение узлов, их особенности по данным ультразвукового осмотра. С этим документом обследуемый направляется к своему лечащему врачу-эндокринологу для решения вопроса о дальнейшей тактике. Если показана операция, то будет назначен оптимальный для нее срок, в противном случае пациент либо будет наблюдаться, периодически проходя УЗ-контроль, либо врач выпишет консервативное медикаментозное лечение.
 Варианты заключений цитолога
Варианты заключений цитолога
Для формулировки заключений цитологи всего мира используют единые международные рекомендации. Эти рекомендации требуют от специалиста максимально точного и краткого заключения, которое даст возможность хирургу или эндокринологу определить единственно верную тактику лечения.
Чтобы устранить значительную изменчивость в сообщениях о цитологических заключениях пункционной биопсии узловых образований щитовидной железы под эгидой Национального Института рака США в 2007 году были представлены согласованные рекомендации, известные как Bethesda System for Reporting Thyroid Cytopathology. Согласно системе Bethesda на основании результата цитологического исследования определяется тактика дальнейшего ведения пациента.
В России также цитологи описывают полученный при пункционной биопсии результат согласно этой системе.
Система цитологических заключений щитовидной железы Bethesda: категории диагностики и риск злокачественности
| Диагностическая категория | Расчетный/
прогнозируемый риск злокачественности |
|
| Bethesda I | Недиагностический / неудовлетворительный Nondiagnostic or unsatisfactory | 1–4 % |
| Bethesda II | Доброкачественный
Benign |
0–3 % |
| Bethesda III | Атипия неопределенного значения / фолликулярное поражение неопределенного значения
Atypia of undetermined significance or follicular lesion of undetermined significance (AUS / FLUS) |
5–15 % |
| Bethesda IV | Фолликулярное новообразование / подозрительное на фолликулярное новообразование
Follicular neoplasm or suspicious for a follicular neoplasm (FN / SFN) |
15–30 % |
| Bethesda V | Подозрительные на злокачественность
Suspicious for malignancy (SUSP) |
60–75 % |
| Bethesda VI | Злокачественная опухоль
Malignan |
97–99 % |
Рекомендации по использованию системы Bethesda Российской ассоциации эндокринологов (2016)
| — неинформативная пункция – вероятность злокачественности – 1 – 4%, рекомендуется повторная ТАБ; |
— доброкачественное образование – вероятность злокачественности – 0 – 4%, рекомендуется динамическое наблюдение. Показания к оперативному лечению при доброкачественном заключении ТАБ:
|
| — атипия неопределенного значения – вероятность злокачественности – 5 – 15%, рекомендуется повторная ТАБ; |
| —атипия неопределенного значения повторно – вероятность злокачественности – 20 –40%, рекомендуется гемитиреоидэктомия с интраоперационным гистологическим исследованием; |
| — фолликулярная неоплазия – вероятность злокачественности – 15 – 30%, рекомендуется гемитиреоидэктомия с интраоперационным гистологическим исследованием; |
| — фолликулярная неоплазия более 5 см – вероятность злокачественности более 50%, в связи с низкой чувствительностью интраоперационного гистологического исследования и высокой вероятностью повторной операции, возможно обсуждение с пациентом целесообразности выполнения тиреоидэктомии; |
| — подозрение на злокачественную опухоль – вероятность злокачественности – 60 – 75%, рекомендуется тиреоидэктомия; |
| — злокачественная опухоль – вероятность злокачественности – 97 – 99%, рекомендуется тиреоидэктомия. |
Рекомендации по использованию системы Bethesda Американской тиреоидологической ассоциации (American Thyroid Association — ATA) (2015)
| Диагностическая категория | Риск злокач. | Тактика |
| Bethesda I | 1-4% | Следует повторить ТАБ, — если возможно с цитологической оценкой на месте.
Если повторная ТАБ недиагностическая, узлы без сонографической картины высокого риска злокачественности требуют тщательного наблюдения. Хирургическое вмешательство следует рассматривать если узел имеет сонографическую картину высокого риска злокачественности, рост узла (> 20% в двух измерениях) или при наличии клинических факторы риска для злокачественного образования. |
| Bethesda II | 0-3% | Узлы с сонографической картиной высокого риска злокачественности – повторить УЗИ и ТАБ в течение 12 месяцев.
Узлы с сонографической картиной низкого и среднего риска злокачественности — повторить УЗИ через 12–24 месяца. Узлы с сонографической картиной очень низкого злокачественности (включая губчатые узлы) -наблюдение. Повторное УЗИ не ранее чем через 24 месяца. Если при повторной ТАБ получен доброкачественный результат наблюдение за узлами для подтверждения риска злокачественности не требуется. |
| Bethesda III | 5-15% | Для узлов с сонографической картиной высокого риска злокачественности – повторная ТАБ или молекулярное тестирование.
Если повторное цитологическое исследование, молекулярное тестирование или и то и другое не выполняются или не дают результатов, может быть выбрано либо наблюдение, либо диагностическая гемитиреоидэктомия в зависимости от клинических факторов риска, сонографических признаков или желания пациента. |
| Bethesda IV | 15-30% | Диагностическое хирургическое иссечение узла ЩЖ – гемитиреоидэктомия.
Тем не менее, возможно отложить оперативное лечение после рассмотрения клинических и сонографических особенностей узла, молекулярного тестирования. Информирование пациента и его мнение должны учитываться для принятия решения. Если нет возможности провести молекулярное тестирование, хирургическое удаление ЩЖ может быть рассмотрено для установления окончательного диагноза. |
| Bethesda V | 60-75% | Хирургическое лечение. Объем операции зависит от клинических факторов риска, сонографических особенностей, предпочтений пациента и, возможно, результатов мутационного тестирования (если оно проводилось).
Предпочтительный объем операции — тиреоидэктомия После рассмотрения клинических и сонографических особенностей мутационное тестирование на BRAF или панель маркеров мутации из семи генов ( BRAF , RAS , RET / PTC , PAX8 / PPARγ ) может быть рассмотрено в узлах с данным цитологическим заключением, если эти данные могут повлиять на принятие клинического решения и выбора объема операции. |
| Bethesda VI | 97-99% | Тиреоидэктомия |
Рекомендации по использованию системы Bethesda Корейской радиологической ассоциацией (Korean Society of Thyroid Radiology (KSThR) (2016)
| Результат ТАБ | Сонографические признаки узла K-TIRADS | Тактика |
| Bethesda-1 | Высокие подозрения
Средний или низкий уровень подозрений |
Повторная ТАБ в течение 3–6 месяцев
Повторная ТАБ в течение 6–12 месяцев |
| Bethesda-2 | Высокие подозрения
Средний или низкий уровень подозрений |
Повторная ТАБ в течение 6–12 месяцев
УЗИ через 12–24 месяца |
| Bethesda-3 | Высокие подозрения
Средний или низкий уровень подозрений. |
Повторная ТАБ в течение 3–6 месяцев
Повторная ТАБ в течение 6–12 месяцев. |
| Bethesda-4 | Все узлы | Диагностическая операция (гемитиреоидэктомия) |
| Bethesda-5 | Высокое или среднее подозрение
Низкое подозрение |
Хирургическое лечение
Повторная ТАБ или оперативное лечение. Активное наблюдение вместо немедленной операции может рассматриваться у взрослых пациентов с вероятной или доказанной папиллярной микрокарциномой |
| Bethesda-6 | Все узлы | Хирургическое лечение.
Активное наблюдение вместо немедленной операции может рассматриваться у взрослых пациентов с вероятной или доказанной папиллярной микрокарциномой |
Представленные рекомендации имеют некоторые отличия, но все они сводятся к тому, что при неинформативном или неопределенном результате необходимо повторить исследование. Если результат пункции не соответствует сонографической картине узла, то пункцию также следует повторить.
Необходимость и сроки повторной пункции должен определить ваш лечащий врач
